
Una revisión actualizada y en profundidad | 09 DIC 18
Histiocitosis de células de Langerhans
Tiene una gran variabilidad en su presentación clínica, desde lesiones indolentes únicas hasta una enfermedad explosiva multisistema
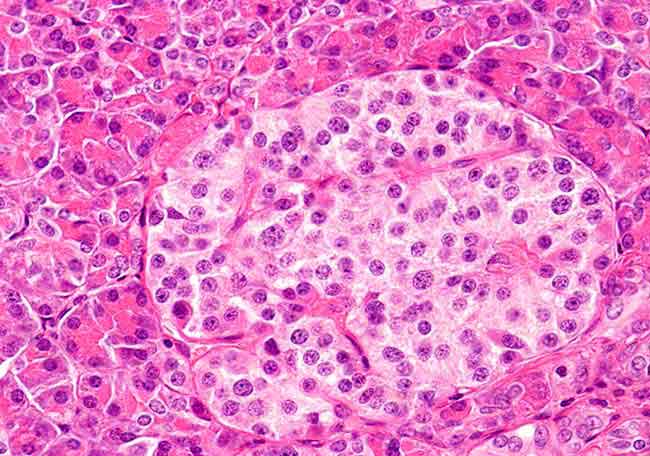
Autor: Carl E. Allen, Miriam Merad, and Kenneth L. McClain N engl j med 379;9
Página 1
Introducción
La histiocitosis de células de Langerhans (HCL), el trastorno histiocítico más común, abarca condiciones caracterizadas por una función y diferenciación o proliferación aberrante de células del sistema de fagocitos mononucleares.
"Histiocito" es un término arcaico (significa "célula de tejido") que se usa para describir las células fagocíticas con características morfológicas mononucleares.1,2 En el caso de la HCL, las lesiones granulomatosas que comprenden histiocitos langerina positivos (CD207+) y un infiltrado inflamatorio pueden surgir en prácticamente cualquier sistema de órganos pero tiene una afinidad particular por los huesos, la piel, los pulmones y la pituitaria.
La HCL tiene una gran variabilidad en su presentación clínica, desde lesiones indolentes únicas hasta una enfermedad explosiva multisistema. Los niños con compromiso de hígado, bazo o médula ósea están en un nivel más alto de riesgo de muerte por HCL y, por lo tanto, se clasifican como que tienen HCL de alto riesgo.3
Aunque los resultados clínicos han mejorado constantemente en las últimas décadas, la quimioterapia estándar (vinblastina, prednisona y mercaptopurina) no logra curar a más del 50% de los niños con enfermedad de alto riesgo, 4 y la mayoría de los pacientes tienen consecuencias a largo plazo, 5 incluyendo un síndrome neurodegenerativo devastador que puede surgir años después de que se presume que un paciente está curado.6,7
En una revisión de 1998, Arceci y colegas capturaron la difícil situación de progreso estancado en la terapia de la HCL llamando al tratamiento empírico una "rueda de ruleta" y observando que la "falta de consenso se deriva de una ambivalencia persistente en cuanto a si la HCL es principalmente un trastorno neoplásico, un trastorno inmunodisregulador o un trastorno con características de ambos.”8
La apariencia histológica benigna de la célula CD207+, el infiltrado inflamatorio acompañante, y las características locales y sistémicas de la tormenta de citoquinas apoya un origen inflamatorio de la HCL, mientras que la clonalidad, la activación somática de mutaciones genéticas en la vía de la proteína quinasa activada por mitógenos (MAPK en inglés), y las mutaciones compartidas con precursores hematopoyéticos favorecen la reclasificación de la HCL como un trastorno neoplásico mieloide.
| La incidencia de HCL es similar a la del linfoma de Hodgkin pediátrico, lo que plantea la pregunta de si la HCL es una enfermedad "huérfana" o uno de los cánceres pediátricos más comunes.9 Esta crisis de identidad no solo ha limitado el desarrollo de estrategias terapéuticas racionales para los pacientes con HCL, sino también ha impedido el acceso a fondos y recursos organizativos que han catalizado los avances en otros trastornos neoplásicos pediátricos.10 |
Aquí los autores revisaron la historia de la HCL y discuten las ideas biológicas recientes que están preparadas para impulsar el tratamiento de la HCL más allá de una ruleta empírica hacia la era de la medicina personalizada.
UNA BREVE HISTORIA
Orígenes de la HCL
Las primeras descripciones de lo que ahora reconocemos como HCL aparecieron a principios del siglo XX como informes de casos y series de casos.
La enfermedad de Hand-Schüller-Christian fue descrita como lesiones óseas líticas granulomatosas eosinófilas, diabetes insípida y exoftalmos en niños jóvenes. 11-13 La enfermedad de Letterer-Siwe fue descrita en lactantes con enfermedad sistémica agresiva y generalmente fatal, incluyendo infiltración de piel, hígado, bazo, y médula por células reticuloendoteliales. 14,15
A mediados del siglo XX, Farber y Lichtenstein señalaron que las muestras de biopsia de casos de enfermedad mortal de Letterer-Siwe y las muestras de casos de granuloma eosinofílico clínicamente leve eran indistinguibles, y los dos patólogos plantearon la hipótesis de que estas condiciones representan manifestaciones de un trastorno común. 16,17 Lichtenstein propuso un diagnóstico común, histiocitosis X, con la X que indica una célula de origen incierto.
Dos décadas después, con el advenimiento de la microscopía electrónica, Nezelof y colegas identificaron un orgánulo intracelular único, el gránulo de Birbeck, en lesiones de histiocitosis X.18 En este punto, los gránulos de Birbeck se pensaba que eran exclusivos de las células epidérmicas de Langerhans, células del sistema fagocítico mononuclear restringidas a la piel.
Se cambió el nombre de histiocitosis X a histiocitosis de células de Langerhans, que refleja el concepto de que las células de la HCL representaban células de Langerhans epidérmicas disfuncionales. Durante las próximas décadas, las revisiones debatieron si la HCL era un desorden de células de Langerhans transformadas o de células de Langerhans normales que se volvieron patológicas por estímulos inapropiados. 8
Langerina, inflamación, e HCL
Las células de Langerhans llevan el nombre de Paul Langerhans, un brillante y joven estudiante de medicina que trabajó con la nueva técnica de tinción coloidal de oro a mediados del siglo XIX.
En 1868, Langerhans describió una población de células epidérmicas, que representaban aproximadamente el 1% de las células epidérmicas, con dendritas características que describió como nervios extracutáneos.20
En 1868, Langerhans describió una población de células epidérmicas, que representaban aproximadamente el 1% de las células epidérmicas, con dendritas características que describió como nervios extracutáneos.20
Ahora sabemos que las células epidérmicas de Langerhans no son nerviosas sino dendríticas, un grupo heterogéneo de células hematopoyéticas enriquecidas en tejidos de interfaz y órganos linfoides.
En la década de 1970, Steinman y Cohn distinguieron células dendríticas de macrófagos en base a las características morfológicas específicas de las células dendríticas y su capacidad superior para presentar antígenos y activar células T antígeno específicas. 21,22
Las células epidérmicas de Langerhans son únicas entre las células dendríticasya que no surgen de las células progenitoras mieloides en médula ósea23 sino de progenitores de saco vitelino y monocitos derivados del hígado fetal que pueblan la piel antes del nacimiento y son mantenidas localmente en condiciones de estado estable.24,25
Sin embargo, en lesiones o inflamación severa, las células derivadas de los monocitos en la sangre periférica tienen el potencial para migrar a la epidermis y diferenciarse en células similares a las células de Langerhans.26
Las células de Langerhans activadas se movilizan a través del receptor de quimioquina CCR7 – dependiente de la migración al drenaje de los ganglios linfáticos, donde presentan antígenos a las células T y finalmente desaparecen a través de la apoptosis y de otros mecanismos.27
Las células de Langerhans epidérmicas inmaduras expresan altos niveles de langerina (CD207), una lectina requerida para la formación de gránulos de Birbeck que inicialmente eran considerados exclusivos de las células de Langerhans.30
Los trastornos histiocíticos se caracterizan generalmente por fenotipo celular: HCL comparte marcadores de superficie con células epidérmicas de Langerhans (CD1a+/CD207+), mientras que los marcadores de superficie del xantogranuloma juvenil y la enfermedad de Erdheim-Chester son más característicos de los macrófagos (CD14+/CD68+/CD163+/factor XIIIa-positivo).
Las lesiones en pacientes con sarcoma histiocítico o histiocitosis maligna son más agresivas que las lesiones de la HCL, con características histológicas de linaje macrófago-monocito, incluyendo positividad para CD68 y CD163 y un índice mitótico más alto.31 En algunos casos, surge un trastorno mixto en el que lesiones separadas tienen fenotipos distintos o una lesión única tiene un fenotipo mixto.32
En lesiones de HCL, las células dendríticas patológicas constituyen menos del 1% a más del 70% de la lesión granulomatosa (mediana, aproximadamente 8%).33 El resto de la lesión está compuesta por infiltrado inflamatorio, incluyendo células T activadas en el fondo de una tormenta de citoquinas.34-36 La desregulación inmune caracteriza claramente los aspectos de la patogénesis de la HCL, aunque los mecanismos que manejan la inflamación permanecen inciertos.
En la década de 1990, Willman y sus colegas investigaron la inactivación no aleatoria del loci del cromosoma X y se encontraron que el porcentaje de células clonales se aproxima al porcentaje de histiocitos CD1a+ en lesiones de pacientes femeninas con HCL.37
Aunque este hallazgo presagiaba la caracterización de la HCL como un trastorno neoplásico mieloide, su importancia biológica siguió siendo incierta por décadas. A pesar de las sugerencias de la clonalidad de las células de Langerhans, 37,38 no hubo evidencia de proliferación dentro de la lesión, 34,36 y no se identificaron alteraciones genómicas macroscópicas.39
COMPRENSIÓN ACTUAL DE LA HCL
Mutaciones de la vía somática MAPK y la HCL
La tecnología genómica mejorada anunció un gran avance en la biología de la HCL. Utilizando la plataforma de pirosecuenciación OncoMap, Badalian-Very y colegas identificaron la mutación BRAF V600E en un el 57% de las lesiones de HCL,40 un hallazgo que posteriormente fue verificado en otras series y atribuido a la célula HCL patógena.33,41-44 BRAF es una quinasa central de la vía de señal de transducción RAS – RAF – MEK que está involucrada en numerosas funciones celulares.
La mutación BRAF V600E hace que la vía MAPK esté constitutivamente activa.46 Aunque las mutaciones somáticas BRAF V600E ocurren en el 7% de todos los cánceres humanos, también se encuentran con frecuencia en condiciones benignas como los nevos melanocíticos y los pólipos del colon.46,47
La secuenciación de todo el exoma ha revelado mutaciones de activación mutuamente exclusivas de la vía MAPK en un paisaje genómico por lo demás tranquilo, sin diferencia significativa en la frecuencia de las mutaciones entre las lesiones de bajo y alto riesgo. 48,49
Además de BRAF V600E, otras mutaciones activadas en BRAF, incluyendo deleciones en marco, fusiones y duplicaciones, han sido informadas en lesiones de HCL. Mutaciones genéticas adicionales de la vía MAPK con función in vitro probada incluyen inserciones o supresiones en exones 2 y 3 de MAP2K1 y raras mutaciones ARAF.44,48-52
La activación de mutaciones somáticas en los genes del receptor tirosina quinasa (ERBB3), NRAS y KRAS también fueron reportados en lesiones de HCL en adultos.44,49,53,54
En una serie institucional, se identificó un activador somático de la mutación en un gen de la vía MAPK en más del 85% de los casos, 51 un hallazgo que está en línea con la señal extracelular universal regulada de la activación de quinasa (ERK) observada en las células de la HCL. 40,49
HCL como una consecuencia de la diferenciación mieloide mal orientada
Los avances en la ontogenia de las células dendríticas y los estudios descriptivos de las células HCL CD207+ fueron difíciles de reconciliar con el modelo de células HCL que representan células de Langerhans epidérmicas transformadas o activadas.
Los subconjuntos de células dendríticas alternativas con el potencial de expresar langerina y formar gránulos de Birbeck se descubrió que estaban en los tejidos en condiciones de estado estacionario y con mayor reclutamiento de sangre a tejido durante la inflamación. 25
La amplia distribución tisular de células dendríticas CD207+ incluye órganos en riesgo de formación de lesiones de HCL, en contraste con el tropismo restringido de las células de Langerhans a la epidermis y a los ganglios linfáticos que drenan la piel.
Además, el perfil de expresión génica de las lesiones HCL CD207+ mostró una superposición mínima con las células de Langerhans epidérmicas, pero mostraron un aumento relativo de la expresión de genes asociados con los precursores de células dendríticas mieloides inmaduros. 36
Una investigación más detallada del estado de diferenciación de las células HCL dentro de las lesiones identificó subpoblaciones heterogéneas CD1a+ con expresión CD207+ variable.55,56 Juntos, estos hallazgos sugirieron que las células de HCL tenían más probabilidades de surgir de una diferenciación desregulada o del reclutamiento de células precursoras derivadas de médula ósea que de células epidérmicas de Langerhans transformadas o activadas.
BRAF V600E proporcionó un biomarcador crítico con el que minar células hematopoyéticas para definir los orígenes de la célula patológica de HCL. Sorprendentemente, las células mutadas BRAF V600E positivas fueron identificadas consistentemente en células mononucleares de sangre periférica (CMSPs) de pacientes de alto riesgo de HCL con lesiones BRAF V600E positivas, aunque las células mutadas constituyeron un porcentaje muy bajo de estas células (típicamente <0,5%).
En comparación las CMSPs BRAF V600E positivas estuvieron casi siempre ausentes en pacientes con HCL activo, de bajo riesgo. Las células mutadas BRAF V600E en sangre localizaban en precursores de células dendríticas CD11c+ y monocitos CD14+.
Además, BRAF V600E fue identificado en células madres hematopoyéticas CD34+ en aspirado de médula ósea de algunos pacientes de alto riesgo, incluyendo muchas células que fueron reportadas como morfológicamente normales.33
La expresión inducida de células BRAF V600E langerina positiva generó lesiones similares a HCL en ratones por otro lado asintomáticos, mientras que la expresión BRAF V600E en precursores de fagocitos mononucleares (que dan lugar a monocitos y células dendríticas) condujeron a enfermedad agresiva y rápidamente fatal, con infiltración difusa del bazo, hígado y médula ósea por células similares a células dendríticas que expresaban CD207+.33
Por lo tanto, los autores tienen la hipótesis de que el estado de diferenciación de la célula precursora en la que surgen las mutaciones sómaticas activadoras de MAPK define la extensión clínica y la severidad de la enfermedad.57
En la propuesta de un modelo de “diferenciación mieloide mal orientada”, las mutaciones activadas MAPK en precursores de células madre hematopoyéticas pluripotentes pueden dar lugar a HCL de alto riesgo, considerando que estas mismas mutaciones en precursores más comprometidos o restringidos a los tejidos pueden dar lugar a HCL multifocal de bajo riesgo, y mutaciones en un precursor local pueden dar lugar a una sola lesión.
En pacientes con activación de mutaciones de MAPK en células madre hematopoyéticas, el porcentaje de células portadoras de la mutación permanece relativamente bajo y estable en el tiempo, con diferenciación sesgada hacia las células HCL patógenas, 33 una observación que proporciona un mayor apoyo para la hipótesis de la diferenciación mieloide mal orientada.
Los patrones de HCL en la piel y el cerebro ofrecen ideas sobre la ontogenia. En el caso de la enfermedad de la piel en los bebés, algunos pacientes tienen una enfermedad limitada a la piel que frecuentemente se resuelve espontáneamente durante un período de varios meses.
Sin embargo, las lesiones de piel, junto con otras lesiones sistémicas en lactantes, pueden convertirse en una enfermedad progresiva, potencialmente mortal que requiere quimioterapia.
En un estudio en lactantes con lesiones cutáneas, las CMSPs BRAF V600E positivas fueron indetectables en casi todos los casos de enfermedad limitada a la piel (incluidos aquellos con lesiones cutáneas BRAF V600E positivas), mientras que las células BRAF V600E positivas se detectaron con frecuencia en la sangre periférica de pacientes con lesiones tanto sistémicas como cutáneas.
Estos hallazgos pueden explicar el fenómeno de la auto resolución de lesiones en algunos lactantes con enfermedad limitada a la piel.45 Como el síndrome mielodisplásico transitorio en niños con trisomía 21 que coincide con la hematopoyesis fetal persistente, la HCL limitada a la piel puede surgir de precursores de células de Langerhans epidérmicas mutadas derivados del hígado fetal que se resuelve con la transición a la hematopoyesis de la médula ósea, por lo que los precursores son indetectables en la circulación.
En aproximadamente el 5% de los pacientes, la neurodegeneración progresiva se desarrolla inicialmente, con cambios de señal características en el tallo cerebral, los ganglios basales, y el cerebelo en las imágenes de la resonancia magnética, seguidos por síntomas clínicos de ataxia, disartria, dismetría, problemas de aprendizaje, y anomalías de comportamiento. 7
Durante años, se pensó que la neurodegeneración asociada a la HCL surgía de la desregulación inmune, en base de estudios de biopsia que muestran células T infiltrantes y la ausencia de células HCL CD1a+/CD207+.58 Sin embargo, se identificó recientemente una baja o ausente expresión de células CD207, BRAF V600E positivas en muestras de biopsia cerebral de pacientes con HCL y neurodegeneración, 19,29 con un nivel extraordinariamente alto de infiltración (>12%) en las regiones afectadas.
La microglia son células mieloides residentes del sistema nervioso central que pueden surgir del saco vitelino durante la gestación.
Mass y colaboradores informaron que los progenitores eritromieloides del saco vitelino con expresión forzada de BRAF V600E podrían poblar el cerebro con microglia BRAF V600E positiva en ratones, con el desarrollo de la neurodegeneración progresiva en adultos.29 Se planteó la hipótesis de que las mutaciones somáticas en el saco vitelino fetal, por lo tanto, representan el origen de la HCL neurodegenerativa.
En un estudio con pacientes con HCL, la persistencia de células BRAF V600E positivas en la sangre periférica después de la quimioterapia en ausencia de lesiones sistémicas de HCL fueron específicas para pacientes con HCL neurodegenerativa.
Además, el examen de muestras de biopsia de cerebro de tales pacientes mostró infiltración perivascular por células BRAF V600E positivas con un fenotipo monocítico (CD14+ CD33+ CD163+ P2RY12−), compatible con que los precursores circulantes son el origen de las células patógenas BRAF V600E positivas.19
Esta observación es consistente con un modelo en el que un clon hematopoyético que causa las lesiones de HCL originales persiste (o reaparece) después de una presunta cura y sirve de reservorio para futuras HCL neurodegenerativas.
Como en el caso de la HCL de la piel, son posibles múltiples orígenes (por ejemplo, saco vitelino y médula ósea).
Características epidemiológicas de la HCL
Se reportó la incidencia anual de HCL de 4,6 casos por 1 millón de niños menores de 15 años, con una proporción hombre-mujer de 1,2:1.59 La incidencia estimada entre adultos es de 1 a 2 casos por millón, aunque la HCL es probablemente infra diagnosticada en esta población.60
La raza y los antecedentes étnicos parecen influir en el riesgo de que se desarrolle la HCL. El registro de estudios en Estados Unidos mostró una mayor incidencia entre los hispanos y una menor incidencia entre los niños negros.61,62
Además, un estudio que involucró pacientes con HCL en Texas mostró que las madres hispanas eran más propensas a tener niños con HCL que las madre no hispanas.63 La HCL puede presentarse antes, después o con otros cánceres histológicos, frecuentemente con mutaciones compartidas que sugieren clonalidad, aunque no está claro si una historia de HCL confiere un aumento del riesgo de cáncer en niños.64,65
ENFOQUES CLÍNICOS ACTUALES
Quimioterapia
A pesar de los avances en desentrañar los mecanismos patogénicos de la HCL, la norma actual de atención de primera línea para la HCL multifocal permanece empíricamente derivada de la quimioterapia
Los resultados generales han mejorado en los ensayos clínicos de HCL desde las décadas pasadas, aunque la supervivencia libre de progresión entre los pacientes de alto riesgo se mantiene en menos del 50%. 3,4,28,66,67
La voluntad de tolerar el fracaso del tratamiento inicial probablemente se deriva de la incertidumbre histórica sobre si considerar a la HCL un cáncer o un trastorno autoinmune, lo que también se refleja en la tendencia a referirse a “reactivación” en lugar de "recaída". Sin embargo, incluso con pacientes de bajo riesgo, para quienes la tasa de mortalidad a corto plazo es baja, el fracaso del tratamiento está asociado con un mayor riesgo de complicaciones a largo plazo, incluyendo la neurodegeneración.5
En el ensayo HCL-III, los niños con HCL de bajo riesgo tratados con vinblastina y prednisona de primera línea por 12 meses tuvieron mayores tasas de supervivencia libre de progresión que los pacientes tratados durante 6 meses (tasa de recaída a los 5 años, 37% vs 54%; P=0,03).4
El potencial de quimioterapia prolongada (12 meses vs 24 meses) para mejorar la supervivencia libre de progresión para pacientes con HCL de alto riesgo se está probando en el ensayo HCL-IV de terapia de primera línea conducido por la Sociedad Histiocítica (Clinical Trials.gov número NCT02205762).
En otro ensayo multicéntrico, el tratamiento de primera línea con vinblastina y prednisona está siendo comparado con la citarabina, sobre la hipótesis de que las células precursoras de la HCL, al igual que los precursores mieloides en los cánceres como la leucemia mieloide aguda, pueden ser sensibles a análogos de nucleósidos (NCT02670707).
Existen pocos datos para guiar la terapia después de que el tratamiento de primera línea ha fallado.
Los análogos de los nucleósidos pueden ser una clase razonable de medicamento para la HCL, aunque queda por definir una dosis óptima. En un ensayo de fase 2, dosis bajas de cladribina rara vez dio lugar a una cura después de 6 meses de terapia.68
Por el contrario, el tratamiento de rescate con cladribina y citarabina, similar al utilizado para el tratamiento de la leucemia aguda, dio lugar a tasas muy altas de curación entre los pacientes de alto riesgo pero se asoció con hospitalización prolongada y altas tasas de muerte relacionadas con el tratamiento.69,70
El trasplante de células hematopoyéticas alogénicas también puede ser curativo para pacientes con HCL refractaria o recidivante: los datos del registro de EE. UU. y Europa desde 2000 hasta 2013 mostró una tasa de supervivencia global de 3 años de 71 al 77%.71 Los datos de series institucionales también muestran resultados prometedores con un enfoque menos agresivo en el que la monoterapia con citarabina o clofarabina se administra en dosis moderadas en el ámbito ambulatorio.72,73
Los datos para orientar la atención clínica de adultos con HCL y aquellos con HCL neurodegenerativa se limitan a estudios de caso y series de casos. Los adultos pueden presentarse con lesiones de fenotipo mixto, que pueden coexistir con otras neoplasias mieloides.
La HCL pulmonar aislada puede desarrollarse en adultos fumadores. La vinblastina y la prednisona pueden estar asociadas con efectos secundarios inaceptables en adultos, y en general, las respuestas a la quimioterapia son menos robustas en adultos que en niños. 74,75
Los abordajes clínicos de la HCL neurodegenerativa históricamente se limitaron por la interpretación de la neurodegeneración como un fenómeno autoinmune o paraneoplásico. Se reportó que la inmunoglobulina intravenosa estabiliza los síntomas.
Sin embargo, si la HCL neurodegenerativa es una manifestación de la inflamación impulsada por células mieloides clonales activadas por MAPK en el sistema nervioso central, la terapia dirigida a la HCL puede ser más apropiada.19,29 De hecho, algunos pacientes con HCL neurodegenerativa tienen respuestas dramáticas a la citarabina o a la terapia dirigida con vemurafenib.19,77
Terapia dirigida
A pesar del descubrimiento de la mutación BRAF V600E en la HCL en 2010 y de la evidencia sustancial que la HCL es impulsada por la activación patológica de MAPK en precursores mieloides, se completaron pocos estudios para guiar el desarrollo de la terapia dirigida en niños.
Los primeros ensayos que involucran adultos con HCL o con la enfermedad de Erdheim–Chester relacionada mostraron respuestas prometedoras a la inhibición de la vía MAPK.
En la fase 1–2 del ensayo “basket” (VE-BASKET) que involucró 14 adultos con HCL BRAF V600E positivo o enfermedad de Erdheim–Chester que podría ser evaluada, el tratamiento con vemurafenib resultó en una tasa de respuesta del 41% según a los Criterios de Evaluación de Respuesta en Tumores Sólidos (RECIST en inglés).78
Por el contrario, un estudio retrospectivo de vemurafenib en 12 adultos con enfermedad de Erdheim–Chester mostró que la tasa de respuesta metabólica (es decir, la proporción de pacientes con captación positiva en la tomografía por emisión de positrones [PET] antes del tratamiento y captación negativa con tratamiento) fue del 100%.79
La diferencia en estos resultados del estudio probablemente reflejan el efecto de inhibición de BRAF V600E sobre la actividad metabólica versus el efecto sobre la citotoxicidad.
En un informe de seguimiento del ensayo VE-BASKET, todos los pacientes con HCL o enfermedad de Erdheim-Chester que podían evaluarse tenían una respuesta metabólica.80 Cómo una respuesta metabólica se traduce en una mejor supervivencia aún no está definido.
Un número limitado de reportes de casos de pacientes pediátricos también sugieren el potencial de respuestas clínicas en niños con HCL refractaria. De forma similar, los primeros informes de casos y series de casos apoyan un beneficio potencial de la inhibición MEK.44,54,81
El potencial de la terapia dirigida a MAPK para curar la HCL es desconocido. En el estudio sobre el resultado a largo plazo después de la interrupción de los inhibidores de Vemurafenib / BRAF en la enfermedad de Erdheim-Chester (LOVE en inglés), la recaída ocurrió en el 75% de los pacientes (adultos con enfermedad de Erdheim-Chester) después de la interrupción de la terapia con inhibidor de BRAF V600E.81
Aunque las células de sangre periférica BRAF V600E positiva y DNA BRAF V600E extracelular circulante en pacientes con enfermedad de alto riesgo son generalmente indetectables con una respuesta completa a la terapia, estos biomarcadores pueden permanecer detectables en pacientes tratados con un inhibidor BRAF V600E, a pesar de las dramáticas respuestas clínicas.19,33,82,83
Esta observación sugiere que los inhibidores de MAPK dirigidos pueden aturdir en lugar de matar a las células precursoras de HCL mutadas. La recolección prospectiva de células de sangre periférica en los ensayos clínicos será valiosa para determinar la utilidad clínica de detectar enfermedad residual mínima para el tratamiento de la HCL.
El perfil de toxicidad indefinido de los agentes que aún se encuentra en fase de evaluación temprana en niños es otro factor que ha desafiado la implementación del tratamiento con inhibidores MAPK en la HCL en pediatría. En estudios con adultos con HCL o enfermedad de Erdheim-Chester, los efectos tóxicos de los inhibidores de MAPK han sido consistentes con aquellos observados en otros ensayos de cáncer.
Se reportaron erupción, artralgias, pirexia, náuseas, vómitos, diarrea, fatiga, y un potencial de un segundo cáncer (más a menudo carcinoma cutáneo de células escamosas) con los inhibidores de BRAF-V600E, y erupción, inflamación oftalmológica, reacción al fármaco con eosinofilia y síntomas sistémicos (DRESS en inglés), rabdomiólisis y neumonitis se observaron con los inhibidores de MEK.78,81,84,85
Una vez que se estableció la seguridad y la eficacia de la monoterapia con inhibidores de MAPK para los niños, estos estudios pueden poner la plataforma para explorar la seguridad y eficacia de combinaciones de los agentes objetivos o la quimioterapia combinados con los inhibidores MAPK.
Estratificación del riesgo molecular
Las mutaciones mutuamente exclusivas de la vía MAPK y ERK activado (fosforilado) han sido identificadas en casi todas las lesiones de HCL. 40,43,49,51 ¿Hay diferencias clínicas predecibles en casos de HCL impulsadas por diferentes mutaciones de MAPK A pesar de que MAPK generalmente se considera una vía lineal (al menos por debajo del nivel de RAF), 86 es posible que mutaciones específicas tengan consecuencias únicas. Los ensayos in vitro de células CD207+ en lesiones primarias de HCL muestran un efecto de mutación específica en la activación de ERK.49
Dos estudios institucionales demostraron que los pacientes con la mutación BRAF V600E tuvieron mayores riesgos de fracaso del tratamiento de primera línea y de HCL neurodegenerativa, aunque los resultados variaron según la relación entre el estado de mutación BRAF y la extensión de la enfermedad en la presentación.33,87 Serán necesarios ensayos prospectivos, incluyendo la evaluación del genotipo de células HCL, para determinar definitivamente el riesgo relativo de diferentes mutaciones en los resultados clínicos en la HCL.
Las diferencias entre los grupos étnicos de Estados Unidos en el riesgo de adquirir HCL sugieren que los factores de riesgo heredados pueden jugar un papel en la susceptibilidad a la HCL y la respuesta a la terapia.61
Además, un estudio de asociación de genoma completo identificó una variante de SMAD6, que codifica un SMAD inhibitorio para señalizar por la proteína morfogenética ósea, transformando el factor de crecimiento β (TGF-β), o ambos, que se asocia con un mayor riesgo de adquirir HCL y es más probable que esté presente en poblaciones hispanas que en otras etnias.88
Si la señalización SMAD6 o TGF-β juega un papel en la patogenia de la HCL no se conoce, pero estos datos, junto con una predisposición a HCL, apuntan a mecanismos patógenos más allá de las mutaciones somáticas en genes MAPK.
OBJETIVOS TERAPÉUTICOS ADICIONALES
Las terapias actuales para la HCL siguen siendo subóptimas. El tratamiento de primera línea con vinblastina y prednisona funciona mal, y aunque la terapia de rescate con altas dosis de análogos de nucleósidos puede ser efectiva, también es altamente tóxica.
Los primeros informes y los ensayos de los inhibidores de BRAF y MEK son prometedores, aunque los efectos secundarios no son triviales y el potencial de cura es incierto. Como los contornos de los mecanismos patogénicos más allá de la activación ERK se completan, deben identificarse oportunidades terapéuticas adicionales.
La vía de señalización MAPK tiene un papel crítico en las funciones celulares, incluyendo la diferenciación celular, la proliferación, y la supervivencia de una manera específica de la célula.47,89 Aunque los primeros estudios identificaron figuras mitóticas en algunas lesiones de HCL y reportaron altos niveles de expresión de Ki67 (un marcador para la proliferación celular), 90 estudios más recientes mostraron que las células epidérmicas normales de Langerhans y las células CD207+ en las lesiones de HCL tienen tasas de proliferación similares.36,61,91
Las células BRAF V600E positivas en general representan menos del 1% del total de las CMSPs y los aspirados de médula ósea en los pacientes de alto riesgo sugieren que un precursor hiperproliferativo es también poco probable.
En ausencia de proliferación aumentada, es plausible que la acumulación y persistencia de células dendríticas patológicas constituyan un mecanismo para la formación de lesiones. BRAF V600E en lesiones CD207+ de HCL inhibe fuertemente la expresión de CCR7, 91 que codifica un receptor de quimioquinas requerido para la migración de las células dendríticas.92
Además, BRAF V600E controla la expresión de BCL2L1, lo que resulta en resistencia a la apoptosis.91 La activación patológica de la señalización de MAPK lleva por lo tanto a la supresión de la migración y a mayor supervivencia de las células dendríticas, con células CD207+ atrapadas en lesiones de HCL y resistentes a la muerte celular. Las estrategias terapéuticas que tienen como objetivo la migración y la supervivencia de las células dendríticas pueden representar nuevos enfoques prometedores.
El porcentaje de células CD207+ en las lesiones de HCL es altamente variable pero generalmente representa una minoría de las células de la lesión, con una mediana del 8% en un estudio.33 En circunstancias normales, las células dendríticas interactúan con las células T para estimular respuestas específicas de antígeno.
Las interacciones funcionales entre células CD207+ y células T infiltrantes de tumores en las lesiones de HCL no están claras, aunque las células CD207+ expresan altos niveles de ligando de muerte programada 1 (PD-L1 en inglés), las células T infiltrantes expresan altos niveles de proteína del receptor coinhibidor de muerte programada 1 (PD-1 en inglés), 93 y los linfocitos infiltrantes están enriquecidos por células T supresoras reguladoras CD4+ activadas. 36,41
Como los mecanismos que impulsan el reclutamiento de células T y la activación están aclarados, la terapia dirigida a los conductores de inflamación local y sistémica puede proporcionar algún beneficio clínico. Un ensayo temprano de talidomida y una serie de casos en los que los pacientes fueron tratados con indometacina sugieren un potencial para respuestas clínicas a agentes antiinflamatorios. 94,95
La interrupción del microambiente inmune también podría explicar el potencial de la inyección local de glucocorticoides o incluso el simple curetaje para curar lesiones óseas aisladas de HCL.
CLASIFICACIÓN
¿Es la HCL un cáncer? La respuesta conlleva importantes implicancias. Hace veinte años, Arceci y colegas especularon que la incertidumbre sobre si la HCL era un cáncer o un trastorno inmunológico llevó al enfoque "ambivalente" de la inmunoquimioterapia para la HCL.8
El tratamiento de primera línea con vinblastina y prednisona sigue siendo el estándar de atención, proporcionando una mejora general de la supervivencia pero aún con altas tasas de fallo del tratamiento.4
Los autores creen que la presencia de mutaciones somáticas activadas de MAPK en células precursoras mieloides resilientes proporciona la base para definir a la HCL como un trastorno neoplásico mieloide.33,57
La Sociedad Histiocitaria también apoya la reclasificación de los trastornos histiocíticos en base a la mutación y al linaje hematopoyético. 97 Esta reinterpretación de la HCL abre oportunidades para ensayos clínicos adicionales realizados por organizaciones de investigación cooperativas en oncología pediátrica para complementar los esfuerzos en curso de la Sociedad Histiocitaria.
CONCLUSIONES
Las perspectivas biológicas sobre la HCL han evolucionado desde notables informes de casos que describen un espectro de patrones de enfermedad a un diagnóstico histológico unificado (histiocitosis X) de estructuras citoplasmáticas compartidas con células de Langerhans epidérmicas (histiocitosis de células de Langerhans).
Los avances clínicos han sido históricamente obstaculizados por los mecanismos indefinidos de la patogenia.
Los avances acelerados en la década pasada han definido a la HCL como un desorden impulsado por la diferenciación mieloide mal orientada, con la extensión de la enfermedad determinada por la célula de origen en la que se surgen mutaciones somáticas activas MAPK. El reto al que nos enfrentamos ahora es traducir el descubrimiento biológico en mejores resultados para niños y adultos con HCL.
Comentario:
La HCL es el trastorno histiocítico más común, con una expresión clínica muy variable, desde lesiones únicas a una enfermedad multisistémica.
En pediatría, los niños con compromiso hepático, de bazo o de médula ósea tienen mayor riesgo de complicaciones y muerte por HCL.
El presente trabajo describe las dificultades en la clasificación de la enfermedad, sugiriendo la tendencia actual a interpretarla como un trastorno neoplásico mieloide. Serán necesarios más estudios para evaluar nuevas formas de tratamiento para mejorar los resultados a corto y largo plazo, aumentando la tasa de curación de los pacientes con HCL.
Resumen y comentario objetivo: Dra. Alejandra Coarasa
Contenidos relacionados
Los editores le recomiendan continuar con las siguientes lecturas:





















.png)










No hay comentarios:
Publicar un comentario