
Posible nueva terapia combinada contra una enfermedad rara de la médula ósea
La mielofibrosis es una enfermedad grave muy poco frecuente que afecta a las células madre de la médula ósea. Un nuevo estudio apunta cómo una terapia combinada con tres fármacos puede mejorar sustancialmente el tratamiento. Ya ha comenzado el ensayo clínico con pacientes de ocho hospitales.
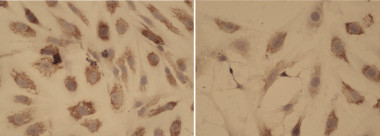
Tinción de colágeno que compara modelos de mielofibrosis. A la izqda., las células sin tratar muestran presencia de fibrosis; a la dcha., células con disminución de la fibrosis tras haber sido sometidas a la terapia. / CNIO
La mielofibrosis es una enfermedad hematológica grave muy poco frecuente, con un tratamiento de eficacia parcial en la actualidad. Su baja incidencia es una de las causas por las que las terapias todavía estén poco desarrolladas.
La Unidad de Investigación Clínica de Tumores Hematológicos H12O-CNIO del Centro Nacional de Investigaciones Oncológicas (CNIO), a la que pertenecen profesionales del Hospital Universitario 12 de Octubre, presenta ahora en la revista Haematologica resultados que abren vías a mejorar sustancialmente el tratamiento de la mielofibrosis, mediante una terapia combinada de tres fármacos. Ya hay en marcha un ensayo clínico con pacientes.
Los resultados abren vías para mejorar sustancialmente el tratamiento de la mielofibrosis, mediante una terapia combinada de tres fármacos
El trabajo ha estado liderado por Joaquín Martínez-López, jefe de la Unidad H120-CNIO y jefe de servicio de Hematología del Hospital Universitario 12 de Octubre, y coordinado por Miguel Gallardo, también de la Unidad H12O-CNIO. Se basa en un cribado farmacológico en que se expone a células de pacientes de mielofibrosis a varios fármacos, entre ellos uno de los tratamientos indicados contra esta enfermedad, el ruxolitinib.
Los resultados muestran que su efecto beneficioso se ve potenciado cuando se combina con nilotinib y prednisona, actualmente en uso contra otras enfermedades.
La mielofibrosis afecta a las células madre de la médula ósea, encargadas de fabricar todas las células de la sangre. Se caracteriza por una producción en exceso de tejido conectivo que desemboca en fibrosis, y que acaba reemplazando a las células madre en la médula.
Esto a su vez fuerza a que la maduración de las células sanguíneas suceda fuera de la médula ósea, y a que células aún sin madurar migren a otros tejidos, como el bazo o el hígado. La edad media de los pacientes en el diagnóstico es de 65 años, aunque la mielofibrosis también se da en jóvenes. La supervivencia con tratamiento es de alrededor de cinco años.
En 2005 se produjo probablemente el avance más importante hasta ahora en la investigación de la mielofibrosis: el descubrimiento de la mutación en el gen JAK2, que junto el hallazgo de la mutación en CALR, en 2013, explican el mecanismo molecular causante de la enfermedad en el 90% de los pacientes.
Gracias a ese hallazgo se empezó a usar el ruxolitinib, que actúa inhibiendo la actividad de la molécula JAK2. Este tratamiento se ha demostrado bastante eficaz en policitemia vera y trombocitemia esencial, patologías que comparten la mutación de JAK2, pero no tanto en mielofibrosis.
Como explica Gallardo, “el ruxolitinib es uno de los tratamientos indicados contra la mielofibrosis, pero, aunque todavía es pronto para evaluar su eficacia en términos de supervivencia, muestra efectividad solo en una parte de los pacientes, e incluso en estos, solo para cierta sintomatología”.
Ante esa situación, la primera firmante del trabajo, Alicia Arenas, del Hospital 12 de Octubre, comenzó hace cinco años explorar la efectividad de otros fármacos ya en uso para otras dolencias, solos o en combinación con el ruxolitinib.
La supervivencia de los pacientes con tratamiento por mielofibrosis es de alrededor de cinco años
Resultados esperanzadores
El grupo seleccionó 17 compuestos cuyo mecanismo de acción o efectos terapéuticos podían encajar como potenciales tratamientos de la mielofibrosis.
Los investigadores generaron ensayos ex vivo con muestras de pacientes de mielofibrosis y empezaron a exponer a las células a los distintos compuestos, de manera aislada y en múltiples combinaciones. Después midieron la efectividad de cada combinación y estudiaron sobre qué vías biológicas estaba actuando cada compuesto.
Los resultados llegan ahora y son esperanzadores. Revelan que en la triple combinación terapéutica de nilotinib y prednisona, junto con el ruxolitinib, “los fármacos se potencian entre ellos”, explica Gallardo, y se logra así “un aumento de la eficacia” del efecto beneficioso del ruxolitinib.
Tal como explican en Haematologica, los autores atribuyen la mejora a la unión del efecto antifibrótico del nilotinib con la acción inmunomoduladora del ruxolitinib y la prednisona, y el anti-proliferativo del ruxolitinib frente al blasto tumoral. La prednisona es un corticoide; el nilotinib se emplea en el tratamiento de la leucemia mieloide crónica.
El hallazgo de su efecto sinérgico contra mielofibrosis ha promovido ya la puesta en marcha de un ensayo clínico fase I para estudiar si las mejoras observadas en cultivos celulares se dan también en pacientes. Participan en el ensayo ocho hospitales españoles.
Referencia bibliográfica:
Alicia Arenas Cortés, Rosa Ayala Díaz, Pilar Hernández-Campo, Julián Gorrochategui, Daniel Primo, Alicia Robles, María Luz Morales, Joan Ballesteros, Inmaculada Rapado, Miguel Gallardo, María Linares, Joaquín Martínez-López. Ruxolitinib in combination with prednisone and nilotinib exhibit synergistic effects in human cells lines and primary cells from myeloproliferative neoplasms. Haematologica 2018. DOI: 10.3324/haematol.2018.201038
El trabajo ha sido financiado por el Instituto de Salud Carlos III, la Fundación CRIS Contra el Cáncer y el Ministerio de Ciencia, Innovación y Universidades.





















.png)










No hay comentarios:
Publicar un comentario