
Fisiopatología, transmisión, clínica y tratamiento | 07 SEP 20
COVID-19: Lo que aprendimos y lo que todavía no sabemos
Los avances en la prevención y el manejo efectivo de COVID-19 requerirán investigación básica y clínica e intervenciones clínicas y de salud pública

Autor/a: W. Wiersinga, A. Rhodes y A. Cheng Fuente: JAMA. 2020;324(8):782-793 Pathophysiology, Transmission, Diagnosis, and Treatment of Coronavirus Disease 2019 (COVID-19)
Introducción
La pandemia de la enfermedad por coronavirus 2019 (COVID-19) ha provocado un aumento repentino y significativo de las hospitalizaciones por neumonía con enfermedad multiorgánica. La infección por SARS-CoV-2 puede ser asintomática o puede causar un amplio espectro de síntomas, como síntomas leves de infección del tracto respiratorio superior y sepsis potencialmente mortal.
Al 1 de julio de 2020, el SARS-CoV-2 ha afectado a más de 200 países, lo que ha resultado en más de 10 millones de casos identificados con 508.000 muertes confirmadas. Esta revisión resume la evidencia actual con respecto a la fisiopatología, transmisión, diagnóstico y tratamiento de COVID-19.
Métodos
Se realizaron búsquedas utilizando los términos de búsqueda coronavirus , síndrome respiratorio agudo severo coronavirus 2 , 2019-nCoV , SARS-CoV-2 , SARS-CoV , MERS-CoV y COVID-19 para los estudios hasta el 15 de junio de 2020, y se buscó manualmente en las referencias de artículos seleccionados artículos relevantes adicionales.
Los autores seleccionaron artículos relevantes para lectores de medicina general, priorizando ensayos clínicos aleatorios, revisiones sistemáticas y guías de práctica clínica.
Observaciones
> Fisiopatología
El SARS-CoV-2 es el tercer coronavirus que ha provocado que una enfermedad grave en los seres humanos se propague a nivel mundial en las últimas 2 décadas. El primer coronavirus que causó una enfermedad grave fue el síndrome respiratorio agudo severo (SARS), que se pensó que se originó en Foshan, China, y resultó en la pandemia de SARS-CoV de 2002-2003. El segundo fue el síndrome respiratorio de Oriente Medio (MERS) causado por el coronavirus, que se originó en la península arábiga en 2012.
A través de la recombinación y la variación genética, los coronavirus pueden adaptarse e infectar a nuevos huéspedes. Se cree que los murciélagos son un reservorio natural del SARS-CoV-2, pero se ha sugerido que los humanos se infectaron con el SARS-CoV-2 a través de un huésped intermedio, como el pangolín.
> La defensa del huésped contra el SARS-CoV-2
Al comienzo de la infección, el SARS-CoV-2 se dirige a las células, como las células epiteliales nasales y bronquiales y los neumocitos, a través de la proteína espiga estructural viral (S) que se une al receptor de la enzima convertidora de angiotensina 2 (ACE2).
La serina proteasa transmembrana de tipo 2 (TMPRSS2), presente en la célula huésped, promueve la captación viral al escindir ACE2 y activar la proteína SARS-CoV-2 S, que media la entrada del coronavirus en las células huésped. ACE2 y TMPRSS2 se expresan en las células diana del hospedador, particularmente en las células epiteliales alveolares de tipo II.
De manera similar a otras enfermedades virales respiratorias, como la influenza, puede ocurrir linfopenia profunda en individuos con COVID-19 cuando el SARS-CoV-2 infecta y mata linfocitos T. Además, la respuesta inflamatoria viral, altera la linfopoyesis y aumenta la apoptosis de los linfocitos.
En etapas posteriores de la infección, cuando se acelera la replicación viral, se compromete la integridad de la barrera epitelial-endotelial. Además de las células epiteliales, el SARS-CoV-2 infecta las células endoteliales capilares pulmonares, lo que acentúa la respuesta inflamatoria y desencadena un influjo de monocitos y neutrófilos.
El angioedema pulmonar dependiente de bradiquinina puede contribuir a la enfermedad. En conjunto, la alteración de la barrera endotelial, la transmisión de oxígeno alveolo-capilar disfuncional y la capacidad de difusión de oxígeno alterada son rasgos característicos de COVID-19.
En el COVID-19 grave, se produce una activación fulminante de la coagulación y el consumo de factores de coagulación. Los tejidos pulmonares inflamados y las células endoteliales pulmonares pueden provocar la formación de microtrombos y contribuir a la alta incidencia de complicaciones trombóticas, como trombosis venosa profunda, embolia pulmonar y complicaciones arteriales trombóticas (isquemia de las extremidades, accidente cerebrovascular isquémico, infarto de miocardio) en situaciones críticas.
El desarrollo de sepsis viral, definida como disfunción orgánica potencialmente mortal causada por una respuesta desregulada del huésped a la infección, puede contribuir aún más al fallo multiorgánico.
> Transmisión de la infección por SARS-CoV-2
Los datos epidemiológicos sugieren que las gotitas expulsadas durante la exposición cara a cara al hablar, toser o estornudar es el modo de transmisión más común (recuadro 1).
La exposición prolongada a una persona infectada (estar dentro de los 2 metros durante al menos 15 minutos) y exposiciones más breves a personas sintomáticas (por ej. personas que tosen) se asocian con un mayor riesgo de transmisión, mientras que las exposiciones breves a contactos asintomáticos tienen menos probabilidades de resultar en transmisión.
La propagación por la superficie de contacto (tocar una superficie con virus) es otro modo posible de transmisión.
La transmisión también puede ocurrir a través de aerosoles (gotitas más pequeñas que permanecen suspendidas en el aire), pero no está claro si esta es una fuente significativa de infección en humanos fuera de un entorno de laboratorio.
Actualmente se cree que el COVID-19 materno está asociado con un riesgo bajo de transmisión vertical. En la mayoría de las series reportadas, la infección de las madres por SARS-CoV-2 ocurrió en el tercer trimestre del embarazo, sin muertes maternas y con un curso clínico favorable en los recién nacidos.
La importancia clínica de la transmisión del SARS-CoV-2 desde superficies inanimadas es difícil de interpretar sin conocer la dosis mínima de partículas virales que pueden iniciar la infección. La carga viral parece persistir a niveles más altos en superficies impermeables, como acero inoxidable y plástico, que en superficies permeables, como cartón.
Se ha identificado el virus en superficies impermeables hasta por 3 a 4 días después de la inoculación. Se ha documentado una contaminación viral generalizada de las habitaciones de los hospitales. Sin embargo, se cree que la cantidad de virus detectada en las superficies decae rápidamente en 48 a 72 horas. El contacto facial sigue siendo el modo principal de transmisión.
La carga viral en el tracto respiratorio superior parece alcanzar su punto máximo alrededor del momento del inicio de los síntomas y la diseminación viral comienza aproximadamente 2 a 3 días antes del inicio de los síntomas.
La diseminación faríngea es alta durante la primera semana de infección en un momento en el que los síntomas aún son leves, lo que podría explicar la transmisión eficiente del SARS-CoV-2, porque las personas infectadas pueden ser infecciosas antes de darse cuenta de que están enfermas.
Aunque los estudios han descrito tasas de infección asintomática que van del 4% al 32%, no está claro si estos informes representan una infección verdaderamente asintomática por personas que nunca desarrollan síntomas, transmisión por personas con síntomas muy leves o transmisión por personas asintomáticas en el momento de la transmisión, pero que posteriormente desarrollan síntomas. Una revisión sistemática sobre este tema sugirió que la verdadera infección asintomática probablemente sea poco común.
Aunque el ácido nucleico viral puede detectarse en frotis de garganta hasta 6 semanas después del inicio de la enfermedad, varios estudios sugieren que los cultivos virales son generalmente negativos para SARS-CoV-2 a los 8 días del inicio de los síntomas. Esto está respaldado por estudios epidemiológicos que han demostrado que la transmisión no ocurrió a los contactos cuya exposición al caso índice comenzó más de 5 días después del inicio de los síntomas en el caso índice.
Presentación clínica
El período de incubación medio (el tiempo desde la exposición hasta el inicio de los síntomas) para COVID-19 es de aproximadamente 5 (rango intercuartil 2-7) días. Aproximadamente el 97,5% de las personas que desarrollan síntomas lo harán dentro de los 11,5 días posteriores a la infección.
El intervalo mediano desde el inicio de los síntomas hasta el ingreso hospitalario es de 7 (3-9) días. La mediana de edad de los pacientes hospitalizados varía entre 47 y 73 años, y la mayoría de las cohortes tienen una preponderancia masculina de aproximadamente el 60%. Entre los pacientes hospitalizados con COVID-19, del 74% al 86% tienen al menos 50 años.
COVID-19 tiene varias manifestaciones clínicas (recuadros 1 y 2).
En un estudio de 44.672 pacientes con COVID-19 en China, el 81% de los pacientes tenían manifestaciones leves, el 14% tenían manifestaciones graves y el 5% tenían manifestaciones críticas (definidas por insuficiencia respiratoria, shock séptico y/o disfunción multiorgánica). Un estudio de 20.133 personas hospitalizadas con COVID-19 en el Reino Unido informó que el 17,1% ingresaron en unidades de cuidados intensivos (UCI).
Aunque la mayoría de los casos pediátricos son leves, un pequeño porcentaje (<7%) de los niños ingresados en el hospital por COVID-19 desarrollan una enfermedad grave que requiere ventilación mecánica. Recientemente se ha descrito un síndrome inflamatorio multisistémico poco común similar a la enfermedad de Kawasaki en niños de Europa y América del Norte con infección por SARS-CoV-2. Este síndrome inflamatorio multisistémico en niños es poco común (2 de cada 100 000 personas <21 años).
Evaluación y diagnóstico
El diagnóstico de COVID-19 generalmente se realiza mediante la prueba de reacción en cadena de la polimerasa mediante hisopo nasal. Sin embargo, debido a las tasas de resultados falsos negativos de las pruebas de PCR del SARS-CoV-2 de los hisopos nasales, los hallazgos clínicos, de laboratorio y de imágenes también pueden usarse para hacer un diagnóstico presuntivo.
> Pruebas de diagnóstico: reacción en cadena de la polimerasa y serología
La detección de ARN del SARS-CoV-2 basada en la reacción en cadena de la polimerasa con transcripción inversa (RT-PCR) a partir de muestras respiratorias (nasofaringe) es el estándar para el diagnóstico. Sin embargo, la sensibilidad de las pruebas varía con el momento de la prueba en relación con la exposición.
Un estudio de modelado estimó la sensibilidad en 33% a los 4 días después de la exposición, 62% el día del inicio de los síntomas y 80% luego de 3 días del inicio de los síntomas. Los factores que contribuyen a los resultados falsos negativos de la prueba incluyen la idoneidad de la técnica de recolección de muestras, el tiempo desde la exposición y la fuente de la muestra.
Las muestras de las vías respiratorias inferiores, como el líquido de lavado broncoalveolar, son más sensibles que las muestras de las vías respiratorias superiores. La saliva puede ser una fuente alternativa de muestras que requiere menos equipo de protección personal y menos hisopos, pero requiere una mayor validación.
Varias pruebas serológicas también pueden ayudar en el diagnóstico y la medición de respuestas a nuevas vacunas. Sin embargo, la presencia de anticuerpos puede no conferir inmunidad porque no todos los anticuerpos producidos en respuesta a la infección son neutralizantes. Se desconoce si se producen segundas infecciones por SARS-CoV-2 y con qué frecuencia. Se desconoce si la presencia de anticuerpos cambia la susceptibilidad a infecciones posteriores o cuánto dura la protección de los anticuerpos.
Los anticuerpos IgM son detectables dentro de los 5 días posteriores a la infección, con niveles más altos de IgM durante las semanas 2 a 3 de la enfermedad, mientras que una respuesta de IgG se observa por primera vez aproximadamente 14 días después del inicio de los síntomas. Los títulos de anticuerpos más altos ocurren con la enfermedad más grave. El rendimiento, la precisión y la validez de estas pruebas son variables.
> Descubrimientos de laboratorio
En una revisión sistemática de 19 estudios de 2.874 pacientes que eran en su mayoría de China, el rango de anomalías de laboratorio observadas incluyeron proteína C reactiva sérica elevada (aumenta en > 60% de los pacientes), lactato deshidrogenasa (aumenta en aproximadamente 50% -60%), ALAT (aumenta en aproximadamente 25%) y ASAT (aproximadamente 33%).
Aproximadamente el 75% de los pacientes tenían albúmina baja.
La anomalía hematológica más común es la linfopenia (recuento absoluto de linfocitos <1,0 × 10 9 / L), que está presente hasta en el 83% de los pacientes hospitalizados con COVID-19.
Junto con la coagulopatía, son frecuentes la prolongación moderada de los tiempos de protrombina (prolongada en> 5% de los pacientes), la trombocitopenia leve (presente en aproximadamente el 30% de los pacientes) y los valores elevados de dímero D (presente en 43% -60% de los pacientes).
Sin embargo, la mayoría de estas características de laboratorio son inespecíficas y son comunes en la neumonía. Las anomalías de laboratorio más graves se han asociado con una infección más grave. El dímero D y, en menor grado, la linfopenia parecen tener las mayores asociaciones pronósticas.
> Imágenes
La anomalía característica de las imágenes en COVID-19 son las opacidades difusas en vidrio esmerilado periférico (ver figura). Las opacidades en vidrio esmerilado tienen márgenes mal definidos, broncograma aéreo, engrosamiento interlobulillar o septal liso o irregular y engrosamiento de la pleura adyacente.
Al comienzo de la enfermedad, los hallazgos de las imágenes de TAC de tórax en aproximadamente el 15% de los individuos y los hallazgos de la Rx de tórax en aproximadamente el 40% de los individuos pueden ser normales.
La rápida evolución de las anomalías puede ocurrir en las primeras dos semanas después del inicio de los síntomas, después de lo cual desaparecen gradualmente. Los hallazgos de las imágenes de TAC de tórax son inespecíficos y se superponen con otras infecciones, por lo que el valor diagnóstico es limitado.
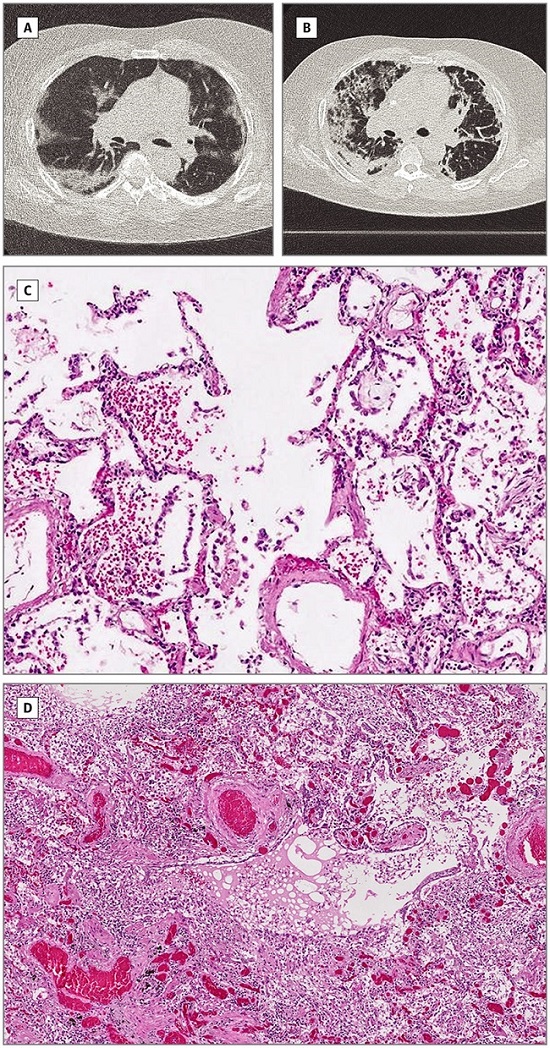
Figura. Hallazgos radiológicos y patológicos pulmonares en COVID-19
Tratamiento
> Tratamiento de sostén y soporte respiratorio
Actualmente, se deben seguir las mejores prácticas para el tratamiento de apoyo de la insuficiencia respiratoria hipóxica aguda y el SDRA. Más del 75% de los pacientes hospitalizados con COVID-19 requieren oxigenoterapia suplementaria.
Para los pacientes que no responden a la terapia de oxígeno convencional, se puede administrar oxígeno de cánula nasal de alto flujo calentado.
Para los pacientes que requieren ventilación mecánica invasiva, se recomienda la ventilación de protección pulmonar con volúmenes corrientes bajos (4-8 ml/kg) y una presión de meseta inferior a 30 mg Hg.
La posición en decúbito prono, una estrategia de presión espiratoria final positiva más alta y el bloqueo neuromuscular a corto plazo con cisatracurio u otros relajantes musculares pueden facilitar la oxigenación.
El umbral para la intubación en la insuficiencia respiratoria relacionada con COVID-19 es controvertido, porque muchos pacientes tienen un trabajo respiratorio normal pero hipoxemia grave. La intubación “más temprana” da tiempo para un proceso de intubación más controlado, lo cual es importante dados los desafíos logísticos de trasladar a los pacientes a una sala de aislamiento aéreo y ponerse el equipo de protección personal antes de la intubación.
Aproximadamente el 8% de los pacientes hospitalizados experimentan una coinfección bacteriana o micótica, pero hasta el 72% son tratados con antibióticos de amplio espectro.
Puede ser prudente evitar los fármacos antibacterianos en pacientes con COVID-19 y reservarlos para aquellos que presenten hallazgos radiológicos y/o marcadores inflamatorios compatibles con coinfección o que estén inmunodeprimidos y/o en estado crítico.
> Apuntando al virus y la respuesta del huésped
Se están evaluando o desarrollando las siguientes clases de medicamentos para el tratamiento de COVID-19: antivirales (por ej., remdesivir, favipiravir), anticuerpos (por ej., plasma de convalecientes, inmunoglobulinas hiperinmunes), agentes antiinflamatorios (dexametasona, estatinas), inmunomoduladores (por ej., tocilizumab, sarilumab, anakinra, ruxolitinib), anticoagulantes (por ej., heparina) y antifibróticos (por ej., inhibidores de tirosina quinasa).
Se han iniciado más de 200 ensayos de cloroquina/hidroxicloroquina, pero los primeros datos no han demostrado un beneficio claro.
Dos estudios retrospectivos no encontraron ningún efecto de la hidroxicloroquina sobre el riesgo de intubación o mortalidad entre los pacientes hospitalizados por COVID-19. Los efectos adversos son frecuentes, sobre todo la prolongación del intervalo QT con un mayor riesgo de complicaciones cardíacas en una población ya vulnerable. Estos hallazgos no apoyan el uso no autorizado de (hidroxi) cloroquina con o sin la coadministración de azitromicina. Los ensayos clínicos aleatorizados están en curso y deberían proporcionar más orientación.
La mayoría de los medicamentos antivirales que se someten a pruebas clínicas en pacientes con COVID-19 son agentes antivirales reutilizados desarrollados originalmente contra la influenza, el VIH, el Ébola o el SARS/MERS.
El uso del inhibidor de la proteasa lopinavir-ritonavir, no mostró beneficios en comparación con la atención estándar en un ensayo aleatorizado, controlado y abierto de 199 pacientes adultos con COVID-19 grave. Entre los inhibidores de la ARN polimerasa que se están evaluando, incluidos ribavirina, favipiravir y remdesivir, este último parece ser el más prometedor.
Los primeros resultados preliminares de un ensayo doble ciego, aleatorizado y controlado con placebo de 1.063 adultos hospitalizados con COVID-19 y evidencia de afectación del tracto respiratorio inferior demostraron que los pacientes aleatorizados para recibir remdesivir tuvieron un tiempo de recuperación más corto que los pacientes del grupo placebo (11 frente a 15 días). El efecto de remdesivir sobre la supervivencia sigue siendo desconocido.
Un primer informe de 5 pacientes críticamente enfermos con COVID-19 tratados con plasma de convalecientes que contiene anticuerpos neutralizantes mostró una mejoría en el estado clínico de todos los participantes.
Sin embargo, un ensayo clínico aleatorizado multicéntrico, abierto y posterior de 103 pacientes en China con COVID-19 grave no encontró diferencias estadísticas en el tiempo hasta la mejoría clínica dentro de los 28 días entre los pacientes aleatorizados para recibir plasma convaleciente frente al tratamiento estándar solo (51,9% vs. 43,1%). Los enfoques alternativos que se están estudiando incluyen el uso de globulina hiperinmune derivada de plasma convaleciente y anticuerpos monoclonales dirigidos contra el SARS-CoV-2.
Los estudios de corticosteroides para la neumonía viral y el SDRA han arrojado resultados mixtos. Sin embargo, el ensayo Randomized Evaluation of COVID-19 Therapy (RECOVERY), que asignó al azar a 2.104 pacientes con COVID-19 para recibir 6 mg diarios de dexametasona durante hasta 10 días y 4.321 para recibir la atención habitual, encontró que la dexametasona redujo la mortalidad diaria por todas las causas (21,6% frente a 24,6%; razón de tasas ajustadas por edad).
El beneficio fue mayor en pacientes con síntomas durante más de 7 días y pacientes que requirieron ventilación mecánica. Por el contrario, no hubo beneficio (y posibilidad de daño) entre los pacientes con síntomas de menor duración y sin necesidad de oxígeno suplementario.
Se recomienda la profilaxis tromboembólica con heparina subcutánea de bajo peso molecular para todos los pacientes hospitalizados con COVID-19. Se están realizando estudios para evaluar si ciertos pacientes (es decir, aquellos con dímero D elevado) se benefician de la anticoagulación terapéutica.
Disparidades
Un porcentaje desproporcionado de hospitalizaciones y muertes por COVID-19 ocurre en minorías y poblaciones de bajos ingresos. Esta carga desproporcionada puede ser un reflejo de disparidades en vivienda, transporte, empleo y salud.
Pronóstico
La mortalidad hospitalaria general por COVID-19 es aproximadamente del 15% al 20%, pero hasta el 40% entre los pacientes que requieren ingreso en la UCI. Sin embargo, las tasas de mortalidad varían entre cohortes, lo que refleja diferencias en la integridad de las pruebas y la identificación de casos, umbrales variables para la hospitalización y diferencias en los resultados.
La mortalidad hospitalaria varía de menos del 5% entre los pacientes menores de 40 años al 35% para los pacientes de 70 a 79 años y más del 60% para los pacientes de 80 a 89 años. Debido a que no todas las personas que mueren durante la pandemia se someten a pruebas de COVID-19, las cifras reales de muertes por COVID-19 son más altas que las registradas.
Prevención y desarrollo de vacunas
COVID-19 es una enfermedad potencialmente prevenible. La relación entre la intensidad de la acción de salud pública y el control de la transmisión se desprende de la epidemiología de la infección en todo el mundo.
Sin embargo, debido a que la mayoría de los países han implementado múltiples medidas de control de infecciones, es difícil determinar el beneficio relativo de cada una. Esta pregunta es cada vez más importante porque se requerirán intervenciones continuas hasta que estén disponibles vacunas o tratamientos eficaces.
En general, estas intervenciones se pueden dividir en aquellas que consisten en acciones personales (distanciamiento físico, higiene personal y uso de equipo de protección), identificación de casos y contactos (ej., prueba-rastreo-rastreo-aislamiento, cierre reactivo de la escuela o del lugar de trabajo ), acciones regulatorias (límites gubernamentales sobre el tamaño de las reuniones o la capacidad empresarial; órdenes para quedarse en casa; cierre o restricción proactiva de escuelas, lugares de trabajo y transporte público; cordon sanitario o cierres de fronteras internas) y medidas fronterizas internacionales (ej., cierre de fronteras o cuarentena forzada).
Una prioridad clave es identificar la combinación de medidas que minimicen los trastornos sociales y económicos al tiempo que controlan adecuadamente la infección. Las medidas óptimas pueden variar entre países según las limitaciones de recursos, la geografía, población y factores políticos (por ej., confianza en el gobierno, diversidad cultural y lingüística).
La evidencia subyacente a estas intervenciones de salud pública no ha cambiado desde la pandemia de gripe de 1918. Los estudios de modelos matemáticos y la evidencia empírica respaldan que las intervenciones de salud pública, incluida la cuarentena domiciliaria después de la infección, la restricción de reuniones masivas, las restricciones de viaje y el distanciamiento social, están asociadas con tasas reducidas de transmisión. El riesgo de resurgimiento surge cuando se levantan estas intervenciones.
Actualmente no se dispone de una vacuna humana para el SARS-CoV-2, pero se están desarrollando aproximadamente 120 candidatos. Los enfoques incluyen el uso de ácidos nucleicos, virus inactivados o atenuados vivos, vectores virales y proteínas recombinantes o partículas virales. Los desafíos para desarrollar una vacuna eficaz consisten en barreras técnicas, viabilidad de producción y regulación a gran escala y barreras legales.
La proteína S de SARS-CoV-2 parece ser un inmunógeno prometedor para la protección, pero no está claro si dirigirse a la proteína completa o solo al dominio de unión al receptor es suficiente para prevenir la transmisión. Otras consideraciones incluyen la duración potencial de la inmunidad y, por lo tanto, el número de dosis de vacuna necesarias para conferir inmunidad.
Es probable que surjan otros enfoques de prevención en los próximos meses, incluidos los anticuerpos monoclonales, la globulina hiperinmune y el plasma convaleciente. Si se demuestra que son efectivos, estos enfoques podrían usarse en personas de alto riesgo, incluidos los trabajadores de la salud, otros trabajadores esenciales y los adultos mayores (en particular, los que se encuentran en hogares de ancianos o con internación a largo plazo).
La pandemia de la enfermedad por coronavirus 2019 (COVID-19) ha provocado un aumento repentino y significativo de las hospitalizaciones por neumonía con enfermedad multiorgánica. La infección por SARS-CoV-2 puede ser asintomática o puede causar un amplio espectro de síntomas, como síntomas leves de infección del tracto respiratorio superior y sepsis potencialmente mortal.
Al 1 de julio de 2020, el SARS-CoV-2 ha afectado a más de 200 países, lo que ha resultado en más de 10 millones de casos identificados con 508.000 muertes confirmadas. Esta revisión resume la evidencia actual con respecto a la fisiopatología, transmisión, diagnóstico y tratamiento de COVID-19.
Métodos
Se realizaron búsquedas utilizando los términos de búsqueda coronavirus , síndrome respiratorio agudo severo coronavirus 2 , 2019-nCoV , SARS-CoV-2 , SARS-CoV , MERS-CoV y COVID-19 para los estudios hasta el 15 de junio de 2020, y se buscó manualmente en las referencias de artículos seleccionados artículos relevantes adicionales.
Los autores seleccionaron artículos relevantes para lectores de medicina general, priorizando ensayos clínicos aleatorios, revisiones sistemáticas y guías de práctica clínica.
Observaciones
> Fisiopatología
El SARS-CoV-2 es el tercer coronavirus que ha provocado que una enfermedad grave en los seres humanos se propague a nivel mundial en las últimas 2 décadas. El primer coronavirus que causó una enfermedad grave fue el síndrome respiratorio agudo severo (SARS), que se pensó que se originó en Foshan, China, y resultó en la pandemia de SARS-CoV de 2002-2003. El segundo fue el síndrome respiratorio de Oriente Medio (MERS) causado por el coronavirus, que se originó en la península arábiga en 2012.
A través de la recombinación y la variación genética, los coronavirus pueden adaptarse e infectar a nuevos huéspedes. Se cree que los murciélagos son un reservorio natural del SARS-CoV-2, pero se ha sugerido que los humanos se infectaron con el SARS-CoV-2 a través de un huésped intermedio, como el pangolín.
> La defensa del huésped contra el SARS-CoV-2
Al comienzo de la infección, el SARS-CoV-2 se dirige a las células, como las células epiteliales nasales y bronquiales y los neumocitos, a través de la proteína espiga estructural viral (S) que se une al receptor de la enzima convertidora de angiotensina 2 (ACE2).
La serina proteasa transmembrana de tipo 2 (TMPRSS2), presente en la célula huésped, promueve la captación viral al escindir ACE2 y activar la proteína SARS-CoV-2 S, que media la entrada del coronavirus en las células huésped. ACE2 y TMPRSS2 se expresan en las células diana del hospedador, particularmente en las células epiteliales alveolares de tipo II.
De manera similar a otras enfermedades virales respiratorias, como la influenza, puede ocurrir linfopenia profunda en individuos con COVID-19 cuando el SARS-CoV-2 infecta y mata linfocitos T. Además, la respuesta inflamatoria viral, altera la linfopoyesis y aumenta la apoptosis de los linfocitos.
| Aunque se ha planteado la hipótesis de que la regulación al alza de los receptores ACE2 de los medicamentos inhibidores de la ECA y bloqueadores del receptor de angiotensina aumenta la susceptibilidad a la infección por SARS-CoV-2, grandes cohortes observacionales no han encontrado una asociación entre estos medicamentos y el riesgo de infección o mortalidad hospitalaria debido a COVID-19. |
Los estudios de autopsia han mostrado un engrosamiento difuso de la pared alveolar con células mononucleares y macrófagos que infiltran los espacios aéreos, además de la endotelitis.Se desarrollan edemas e infiltrados inflamatorios mononucleares intersticiales que aparecen como opacidades en vidrio esmerilado en la imagen por tomografía computada. A continuación, se produce un edema pulmonar que llena los espacios alveolares con la formación de una membrana hialina, compatible con el síndrome de dificultad respiratoria aguda (SDRA) de fase temprana.
El angioedema pulmonar dependiente de bradiquinina puede contribuir a la enfermedad. En conjunto, la alteración de la barrera endotelial, la transmisión de oxígeno alveolo-capilar disfuncional y la capacidad de difusión de oxígeno alterada son rasgos característicos de COVID-19.
En el COVID-19 grave, se produce una activación fulminante de la coagulación y el consumo de factores de coagulación. Los tejidos pulmonares inflamados y las células endoteliales pulmonares pueden provocar la formación de microtrombos y contribuir a la alta incidencia de complicaciones trombóticas, como trombosis venosa profunda, embolia pulmonar y complicaciones arteriales trombóticas (isquemia de las extremidades, accidente cerebrovascular isquémico, infarto de miocardio) en situaciones críticas.
El desarrollo de sepsis viral, definida como disfunción orgánica potencialmente mortal causada por una respuesta desregulada del huésped a la infección, puede contribuir aún más al fallo multiorgánico.
> Transmisión de la infección por SARS-CoV-2
Los datos epidemiológicos sugieren que las gotitas expulsadas durante la exposición cara a cara al hablar, toser o estornudar es el modo de transmisión más común (recuadro 1).
La exposición prolongada a una persona infectada (estar dentro de los 2 metros durante al menos 15 minutos) y exposiciones más breves a personas sintomáticas (por ej. personas que tosen) se asocian con un mayor riesgo de transmisión, mientras que las exposiciones breves a contactos asintomáticos tienen menos probabilidades de resultar en transmisión.
La propagación por la superficie de contacto (tocar una superficie con virus) es otro modo posible de transmisión.
La transmisión también puede ocurrir a través de aerosoles (gotitas más pequeñas que permanecen suspendidas en el aire), pero no está claro si esta es una fuente significativa de infección en humanos fuera de un entorno de laboratorio.
Actualmente se cree que el COVID-19 materno está asociado con un riesgo bajo de transmisión vertical. En la mayoría de las series reportadas, la infección de las madres por SARS-CoV-2 ocurrió en el tercer trimestre del embarazo, sin muertes maternas y con un curso clínico favorable en los recién nacidos.
Recuadro 1. Transmisión, síntomas y complicaciones de la enfermedad por coronavirus 2019 (COVID-19)
|
Se ha identificado el virus en superficies impermeables hasta por 3 a 4 días después de la inoculación. Se ha documentado una contaminación viral generalizada de las habitaciones de los hospitales. Sin embargo, se cree que la cantidad de virus detectada en las superficies decae rápidamente en 48 a 72 horas. El contacto facial sigue siendo el modo principal de transmisión.
La carga viral en el tracto respiratorio superior parece alcanzar su punto máximo alrededor del momento del inicio de los síntomas y la diseminación viral comienza aproximadamente 2 a 3 días antes del inicio de los síntomas.
La diseminación faríngea es alta durante la primera semana de infección en un momento en el que los síntomas aún son leves, lo que podría explicar la transmisión eficiente del SARS-CoV-2, porque las personas infectadas pueden ser infecciosas antes de darse cuenta de que están enfermas.
Aunque los estudios han descrito tasas de infección asintomática que van del 4% al 32%, no está claro si estos informes representan una infección verdaderamente asintomática por personas que nunca desarrollan síntomas, transmisión por personas con síntomas muy leves o transmisión por personas asintomáticas en el momento de la transmisión, pero que posteriormente desarrollan síntomas. Una revisión sistemática sobre este tema sugirió que la verdadera infección asintomática probablemente sea poco común.
Aunque el ácido nucleico viral puede detectarse en frotis de garganta hasta 6 semanas después del inicio de la enfermedad, varios estudios sugieren que los cultivos virales son generalmente negativos para SARS-CoV-2 a los 8 días del inicio de los síntomas. Esto está respaldado por estudios epidemiológicos que han demostrado que la transmisión no ocurrió a los contactos cuya exposición al caso índice comenzó más de 5 días después del inicio de los síntomas en el caso índice.
Esto sugiere que los individuos pueden salir del aislamiento en función de la mejoría clínica.Los Centros para el CDCs recomiendan el aislamiento durante al menos 10 días después de la aparición de los síntomas y 3 días después de la mejora de los síntomas. Sigue habiendo incertidumbre acerca de si se requieren pruebas seriadas para subgrupos específicos, como pacientes inmunosuprimidos o pacientes críticamente enfermos para quienes la resolución de los síntomas puede demorarse o adultos mayores.
Presentación clínica
El período de incubación medio (el tiempo desde la exposición hasta el inicio de los síntomas) para COVID-19 es de aproximadamente 5 (rango intercuartil 2-7) días. Aproximadamente el 97,5% de las personas que desarrollan síntomas lo harán dentro de los 11,5 días posteriores a la infección.
El intervalo mediano desde el inicio de los síntomas hasta el ingreso hospitalario es de 7 (3-9) días. La mediana de edad de los pacientes hospitalizados varía entre 47 y 73 años, y la mayoría de las cohortes tienen una preponderancia masculina de aproximadamente el 60%. Entre los pacientes hospitalizados con COVID-19, del 74% al 86% tienen al menos 50 años.
COVID-19 tiene varias manifestaciones clínicas (recuadros 1 y 2).
En un estudio de 44.672 pacientes con COVID-19 en China, el 81% de los pacientes tenían manifestaciones leves, el 14% tenían manifestaciones graves y el 5% tenían manifestaciones críticas (definidas por insuficiencia respiratoria, shock séptico y/o disfunción multiorgánica). Un estudio de 20.133 personas hospitalizadas con COVID-19 en el Reino Unido informó que el 17,1% ingresaron en unidades de cuidados intensivos (UCI).
Recuadro 2. Preguntas frecuentes sobre la enfermedad por coronavirus 2019 (COVID-19)
|
- Aproximadamente del 17% al 35% de los pacientes hospitalizados con COVID-19 son tratados en una UCI, con mayor frecuencia debido a insuficiencia respiratoria hipoxémica.
- Entre los pacientes en la UCI con COVID-19, del 29% al 91% requieren ventilación mecánica invasiva.
- Además de insuficiencia respiratoria, los pacientes hospitalizados pueden desarrollar insuficiencia renal aguda (9%), disfunción hepática (19%), disfunción hemorrágica y de coagulación (10-25%) y shock séptico (6%).
- Aproximadamente del 2% al 5% de las personas con COVID-19 confirmado por laboratorio son menores de 18 años, con una mediana de edad de 11 años.
Aunque la mayoría de los casos pediátricos son leves, un pequeño porcentaje (<7%) de los niños ingresados en el hospital por COVID-19 desarrollan una enfermedad grave que requiere ventilación mecánica. Recientemente se ha descrito un síndrome inflamatorio multisistémico poco común similar a la enfermedad de Kawasaki en niños de Europa y América del Norte con infección por SARS-CoV-2. Este síndrome inflamatorio multisistémico en niños es poco común (2 de cada 100 000 personas <21 años).
Evaluación y diagnóstico
El diagnóstico de COVID-19 generalmente se realiza mediante la prueba de reacción en cadena de la polimerasa mediante hisopo nasal. Sin embargo, debido a las tasas de resultados falsos negativos de las pruebas de PCR del SARS-CoV-2 de los hisopos nasales, los hallazgos clínicos, de laboratorio y de imágenes también pueden usarse para hacer un diagnóstico presuntivo.
> Pruebas de diagnóstico: reacción en cadena de la polimerasa y serología
La detección de ARN del SARS-CoV-2 basada en la reacción en cadena de la polimerasa con transcripción inversa (RT-PCR) a partir de muestras respiratorias (nasofaringe) es el estándar para el diagnóstico. Sin embargo, la sensibilidad de las pruebas varía con el momento de la prueba en relación con la exposición.
Un estudio de modelado estimó la sensibilidad en 33% a los 4 días después de la exposición, 62% el día del inicio de los síntomas y 80% luego de 3 días del inicio de los síntomas. Los factores que contribuyen a los resultados falsos negativos de la prueba incluyen la idoneidad de la técnica de recolección de muestras, el tiempo desde la exposición y la fuente de la muestra.
Las muestras de las vías respiratorias inferiores, como el líquido de lavado broncoalveolar, son más sensibles que las muestras de las vías respiratorias superiores. La saliva puede ser una fuente alternativa de muestras que requiere menos equipo de protección personal y menos hisopos, pero requiere una mayor validación.
Varias pruebas serológicas también pueden ayudar en el diagnóstico y la medición de respuestas a nuevas vacunas. Sin embargo, la presencia de anticuerpos puede no conferir inmunidad porque no todos los anticuerpos producidos en respuesta a la infección son neutralizantes. Se desconoce si se producen segundas infecciones por SARS-CoV-2 y con qué frecuencia. Se desconoce si la presencia de anticuerpos cambia la susceptibilidad a infecciones posteriores o cuánto dura la protección de los anticuerpos.
Los anticuerpos IgM son detectables dentro de los 5 días posteriores a la infección, con niveles más altos de IgM durante las semanas 2 a 3 de la enfermedad, mientras que una respuesta de IgG se observa por primera vez aproximadamente 14 días después del inicio de los síntomas. Los títulos de anticuerpos más altos ocurren con la enfermedad más grave. El rendimiento, la precisión y la validez de estas pruebas son variables.
> Descubrimientos de laboratorio
En una revisión sistemática de 19 estudios de 2.874 pacientes que eran en su mayoría de China, el rango de anomalías de laboratorio observadas incluyeron proteína C reactiva sérica elevada (aumenta en > 60% de los pacientes), lactato deshidrogenasa (aumenta en aproximadamente 50% -60%), ALAT (aumenta en aproximadamente 25%) y ASAT (aproximadamente 33%).
Aproximadamente el 75% de los pacientes tenían albúmina baja.
La anomalía hematológica más común es la linfopenia (recuento absoluto de linfocitos <1,0 × 10 9 / L), que está presente hasta en el 83% de los pacientes hospitalizados con COVID-19.
Junto con la coagulopatía, son frecuentes la prolongación moderada de los tiempos de protrombina (prolongada en> 5% de los pacientes), la trombocitopenia leve (presente en aproximadamente el 30% de los pacientes) y los valores elevados de dímero D (presente en 43% -60% de los pacientes).
Sin embargo, la mayoría de estas características de laboratorio son inespecíficas y son comunes en la neumonía. Las anomalías de laboratorio más graves se han asociado con una infección más grave. El dímero D y, en menor grado, la linfopenia parecen tener las mayores asociaciones pronósticas.
> Imágenes
La anomalía característica de las imágenes en COVID-19 son las opacidades difusas en vidrio esmerilado periférico (ver figura). Las opacidades en vidrio esmerilado tienen márgenes mal definidos, broncograma aéreo, engrosamiento interlobulillar o septal liso o irregular y engrosamiento de la pleura adyacente.
Al comienzo de la enfermedad, los hallazgos de las imágenes de TAC de tórax en aproximadamente el 15% de los individuos y los hallazgos de la Rx de tórax en aproximadamente el 40% de los individuos pueden ser normales.
La rápida evolución de las anomalías puede ocurrir en las primeras dos semanas después del inicio de los síntomas, después de lo cual desaparecen gradualmente. Los hallazgos de las imágenes de TAC de tórax son inespecíficos y se superponen con otras infecciones, por lo que el valor diagnóstico es limitado.

Figura. Hallazgos radiológicos y patológicos pulmonares en COVID-19
Tratamiento
> Tratamiento de sostén y soporte respiratorio
Actualmente, se deben seguir las mejores prácticas para el tratamiento de apoyo de la insuficiencia respiratoria hipóxica aguda y el SDRA. Más del 75% de los pacientes hospitalizados con COVID-19 requieren oxigenoterapia suplementaria.
Para los pacientes que no responden a la terapia de oxígeno convencional, se puede administrar oxígeno de cánula nasal de alto flujo calentado.
Para los pacientes que requieren ventilación mecánica invasiva, se recomienda la ventilación de protección pulmonar con volúmenes corrientes bajos (4-8 ml/kg) y una presión de meseta inferior a 30 mg Hg.
La posición en decúbito prono, una estrategia de presión espiratoria final positiva más alta y el bloqueo neuromuscular a corto plazo con cisatracurio u otros relajantes musculares pueden facilitar la oxigenación.
El umbral para la intubación en la insuficiencia respiratoria relacionada con COVID-19 es controvertido, porque muchos pacientes tienen un trabajo respiratorio normal pero hipoxemia grave. La intubación “más temprana” da tiempo para un proceso de intubación más controlado, lo cual es importante dados los desafíos logísticos de trasladar a los pacientes a una sala de aislamiento aéreo y ponerse el equipo de protección personal antes de la intubación.
Sin embargo, la hipoxemia en ausencia de dificultad respiratoria se tolera bien y los pacientes pueden evolucionar bien sin ventilación mecánica.Los umbrales de intubación más tempranos pueden resultar en tratar a algunos pacientes con ventilación mecánica innecesariamente y exponerlos a complicaciones adicionales. Actualmente, no existe evidencia suficiente para hacer recomendaciones con respecto a la intubación más temprana frente a la posterior.
Aproximadamente el 8% de los pacientes hospitalizados experimentan una coinfección bacteriana o micótica, pero hasta el 72% son tratados con antibióticos de amplio espectro.
Puede ser prudente evitar los fármacos antibacterianos en pacientes con COVID-19 y reservarlos para aquellos que presenten hallazgos radiológicos y/o marcadores inflamatorios compatibles con coinfección o que estén inmunodeprimidos y/o en estado crítico.
> Apuntando al virus y la respuesta del huésped
Se están evaluando o desarrollando las siguientes clases de medicamentos para el tratamiento de COVID-19: antivirales (por ej., remdesivir, favipiravir), anticuerpos (por ej., plasma de convalecientes, inmunoglobulinas hiperinmunes), agentes antiinflamatorios (dexametasona, estatinas), inmunomoduladores (por ej., tocilizumab, sarilumab, anakinra, ruxolitinib), anticoagulantes (por ej., heparina) y antifibróticos (por ej., inhibidores de tirosina quinasa).
Es probable que diferentes modalidades de tratamiento tengan diferente eficacia en diferentes etapas de la enfermedad y en diferentes manifestaciones de la enfermedad.Se esperaría que la inhibición viral sea más eficaz en las primeras etapas de la infección, mientras que, en pacientes hospitalizados, los agentes inmunomoduladores pueden ser útiles para prevenir la progresión de la enfermedad y los anticoagulantes pueden ser útiles para prevenir complicaciones tromboembólicas.
Se han iniciado más de 200 ensayos de cloroquina/hidroxicloroquina, pero los primeros datos no han demostrado un beneficio claro.
Dos estudios retrospectivos no encontraron ningún efecto de la hidroxicloroquina sobre el riesgo de intubación o mortalidad entre los pacientes hospitalizados por COVID-19. Los efectos adversos son frecuentes, sobre todo la prolongación del intervalo QT con un mayor riesgo de complicaciones cardíacas en una población ya vulnerable. Estos hallazgos no apoyan el uso no autorizado de (hidroxi) cloroquina con o sin la coadministración de azitromicina. Los ensayos clínicos aleatorizados están en curso y deberían proporcionar más orientación.
La mayoría de los medicamentos antivirales que se someten a pruebas clínicas en pacientes con COVID-19 son agentes antivirales reutilizados desarrollados originalmente contra la influenza, el VIH, el Ébola o el SARS/MERS.
El uso del inhibidor de la proteasa lopinavir-ritonavir, no mostró beneficios en comparación con la atención estándar en un ensayo aleatorizado, controlado y abierto de 199 pacientes adultos con COVID-19 grave. Entre los inhibidores de la ARN polimerasa que se están evaluando, incluidos ribavirina, favipiravir y remdesivir, este último parece ser el más prometedor.
Los primeros resultados preliminares de un ensayo doble ciego, aleatorizado y controlado con placebo de 1.063 adultos hospitalizados con COVID-19 y evidencia de afectación del tracto respiratorio inferior demostraron que los pacientes aleatorizados para recibir remdesivir tuvieron un tiempo de recuperación más corto que los pacientes del grupo placebo (11 frente a 15 días). El efecto de remdesivir sobre la supervivencia sigue siendo desconocido.
Un primer informe de 5 pacientes críticamente enfermos con COVID-19 tratados con plasma de convalecientes que contiene anticuerpos neutralizantes mostró una mejoría en el estado clínico de todos los participantes.
Sin embargo, un ensayo clínico aleatorizado multicéntrico, abierto y posterior de 103 pacientes en China con COVID-19 grave no encontró diferencias estadísticas en el tiempo hasta la mejoría clínica dentro de los 28 días entre los pacientes aleatorizados para recibir plasma convaleciente frente al tratamiento estándar solo (51,9% vs. 43,1%). Los enfoques alternativos que se están estudiando incluyen el uso de globulina hiperinmune derivada de plasma convaleciente y anticuerpos monoclonales dirigidos contra el SARS-CoV-2.
Las estrategias terapéuticas alternativas consisten en modular la respuesta inflamatoria en pacientes con COVID-19.Los anticuerpos monoclonales dirigidos contra mediadores inflamatorios clave, como el interferón gamma, la IL-1, la IL-6 y el factor del complemento 5a, se dirigen todos a la respuesta inflamatoria abrumadora que sigue a la infección por SARS-CoV-2 con el objetivo de prevenir el daño orgánico. De estos, los inhibidores de la IL-6 tocilizumab y sarilumab son los que mejor se estudian. Los inhibidores de la tirosina quinasa, como el imatinib, se estudian por su potencial para prevenir la fuga vascular pulmonar en personas con COVID-19.
Los estudios de corticosteroides para la neumonía viral y el SDRA han arrojado resultados mixtos. Sin embargo, el ensayo Randomized Evaluation of COVID-19 Therapy (RECOVERY), que asignó al azar a 2.104 pacientes con COVID-19 para recibir 6 mg diarios de dexametasona durante hasta 10 días y 4.321 para recibir la atención habitual, encontró que la dexametasona redujo la mortalidad diaria por todas las causas (21,6% frente a 24,6%; razón de tasas ajustadas por edad).
El beneficio fue mayor en pacientes con síntomas durante más de 7 días y pacientes que requirieron ventilación mecánica. Por el contrario, no hubo beneficio (y posibilidad de daño) entre los pacientes con síntomas de menor duración y sin necesidad de oxígeno suplementario.
Se recomienda la profilaxis tromboembólica con heparina subcutánea de bajo peso molecular para todos los pacientes hospitalizados con COVID-19. Se están realizando estudios para evaluar si ciertos pacientes (es decir, aquellos con dímero D elevado) se benefician de la anticoagulación terapéutica.
Disparidades
Un porcentaje desproporcionado de hospitalizaciones y muertes por COVID-19 ocurre en minorías y poblaciones de bajos ingresos. Esta carga desproporcionada puede ser un reflejo de disparidades en vivienda, transporte, empleo y salud.
Pronóstico
La mortalidad hospitalaria general por COVID-19 es aproximadamente del 15% al 20%, pero hasta el 40% entre los pacientes que requieren ingreso en la UCI. Sin embargo, las tasas de mortalidad varían entre cohortes, lo que refleja diferencias en la integridad de las pruebas y la identificación de casos, umbrales variables para la hospitalización y diferencias en los resultados.
La mortalidad hospitalaria varía de menos del 5% entre los pacientes menores de 40 años al 35% para los pacientes de 70 a 79 años y más del 60% para los pacientes de 80 a 89 años. Debido a que no todas las personas que mueren durante la pandemia se someten a pruebas de COVID-19, las cifras reales de muertes por COVID-19 son más altas que las registradas.
Aunque actualmente se desconocen los resultados a largo plazo de COVID-19, es probable que los pacientes con enfermedades graves sufran secuelas importantes.La supervivencia de la sepsis se asocia con un mayor riesgo de mortalidad durante al menos 2 años, una nueva discapacidad física, un nuevo deterioro cognitivo y una mayor vulnerabilidad a infecciones recurrentes y un mayor deterioro de la salud. Es probable que se observen secuelas similares en los sobrevivientes de COVID-19 grave.
Prevención y desarrollo de vacunas
COVID-19 es una enfermedad potencialmente prevenible. La relación entre la intensidad de la acción de salud pública y el control de la transmisión se desprende de la epidemiología de la infección en todo el mundo.
Sin embargo, debido a que la mayoría de los países han implementado múltiples medidas de control de infecciones, es difícil determinar el beneficio relativo de cada una. Esta pregunta es cada vez más importante porque se requerirán intervenciones continuas hasta que estén disponibles vacunas o tratamientos eficaces.
En general, estas intervenciones se pueden dividir en aquellas que consisten en acciones personales (distanciamiento físico, higiene personal y uso de equipo de protección), identificación de casos y contactos (ej., prueba-rastreo-rastreo-aislamiento, cierre reactivo de la escuela o del lugar de trabajo ), acciones regulatorias (límites gubernamentales sobre el tamaño de las reuniones o la capacidad empresarial; órdenes para quedarse en casa; cierre o restricción proactiva de escuelas, lugares de trabajo y transporte público; cordon sanitario o cierres de fronteras internas) y medidas fronterizas internacionales (ej., cierre de fronteras o cuarentena forzada).
Una prioridad clave es identificar la combinación de medidas que minimicen los trastornos sociales y económicos al tiempo que controlan adecuadamente la infección. Las medidas óptimas pueden variar entre países según las limitaciones de recursos, la geografía, población y factores políticos (por ej., confianza en el gobierno, diversidad cultural y lingüística).
La evidencia subyacente a estas intervenciones de salud pública no ha cambiado desde la pandemia de gripe de 1918. Los estudios de modelos matemáticos y la evidencia empírica respaldan que las intervenciones de salud pública, incluida la cuarentena domiciliaria después de la infección, la restricción de reuniones masivas, las restricciones de viaje y el distanciamiento social, están asociadas con tasas reducidas de transmisión. El riesgo de resurgimiento surge cuando se levantan estas intervenciones.
Actualmente no se dispone de una vacuna humana para el SARS-CoV-2, pero se están desarrollando aproximadamente 120 candidatos. Los enfoques incluyen el uso de ácidos nucleicos, virus inactivados o atenuados vivos, vectores virales y proteínas recombinantes o partículas virales. Los desafíos para desarrollar una vacuna eficaz consisten en barreras técnicas, viabilidad de producción y regulación a gran escala y barreras legales.
La proteína S de SARS-CoV-2 parece ser un inmunógeno prometedor para la protección, pero no está claro si dirigirse a la proteína completa o solo al dominio de unión al receptor es suficiente para prevenir la transmisión. Otras consideraciones incluyen la duración potencial de la inmunidad y, por lo tanto, el número de dosis de vacuna necesarias para conferir inmunidad.
Es probable que surjan otros enfoques de prevención en los próximos meses, incluidos los anticuerpos monoclonales, la globulina hiperinmune y el plasma convaleciente. Si se demuestra que son efectivos, estos enfoques podrían usarse en personas de alto riesgo, incluidos los trabajadores de la salud, otros trabajadores esenciales y los adultos mayores (en particular, los que se encuentran en hogares de ancianos o con internación a largo plazo).
| Conclusiones Al 1 de julio de 2020, más de 10 millones de personas en todo el mundo habían sido infectadas con SARS-CoV-2. Muchos aspectos de la transmisión, la infección y el tratamiento siguen sin estar claros. Los avances en la prevención y el manejo efectivo de COVID-19 requerirán investigación básica y clínica e intervenciones clínicas y de salud pública. |





















.png)










No hay comentarios:
Publicar un comentario