
Gran impacto en la calidad de vida | 13 SEP 20
Neuralgia del trigémino
La neuralgia del trigémino es una afección extremadamente dolorosa que puede ser difícil de diagnosticar y tratar

Autor/a: G. Cruccu, G. Di Stefano y A. Truini Fuente: N Engl J Med 2020; 383: 754-762 Trigeminal Neuralgia
Introducción
La neuralgia del trigémino, tradicionalmente llamada tic doloroso, es un trastorno de dolor neuropático crónico caracterizado por paroxismos espontáneos y provocados de dolor punzante o similar a una descarga eléctrica en una región de la cara. Se han atribuido al trastorno una mala calidad de vida y el suicidio en casos graves.
Características clínicas y diagnóstico
El diagnóstico de neuralgia del trigémino es clínico y se basa en tres criterios principales:
El dolor de la neuralgia del trigémino afecta con mayor frecuencia la distribución de la segunda (maxilar) o tercer (mandibular) división del nervio trigémino, afectando el lado derecho de la cara con más frecuencia que el lado izquierdo.
La neuralgia bilateral del trigémino es poco común y debe suscitar preocupación por la posibilidad de neuralgia facial debida a una enfermedad neurológica subyacente o un trastorno no neurológico que afecta al cráneo.
El tercio posterior del cuero cabelludo, el oído externo (a excepción del trago) y la piel que recubre el ángulo de la mandíbula no están inervados por el nervio trigémino y no son sitios de dolor debido a la neuralgia del trigémino (ver figura a continuación); el dolor en estas áreas sugiere un proceso diferente.
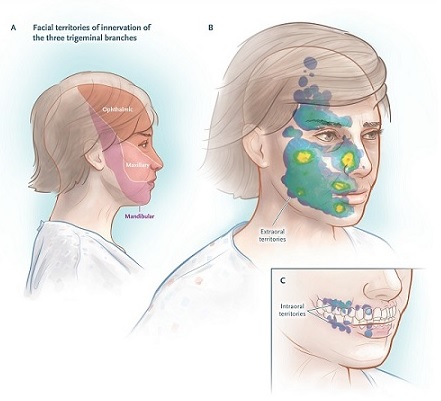
Territorios de inervación del nervio trigémino y distribución de la zona de activación.El dolor de la neuralgia del trigémino puede desencadenarse por gestos comunes de la vida diaria, y los desencadenantes se encuentran en pequeñas zonas sensoriales receptivas, por ejemplo, el toque de una servilleta o tejido en el labio superior o incluso una brisa que fluye a través de un área sensible de la cara.
La ubicación del dolor no siempre es concordante con el lugar del desencadenante sensorial. Por ejemplo, los estímulos en y alrededor del labio inferior pueden inducir dolor en la sien, o los desencadenantes sensoriales en las porciones laterales de la nariz pueden inducir un dolor similar a un choque que se irradia hacia la frente o el labio superior.
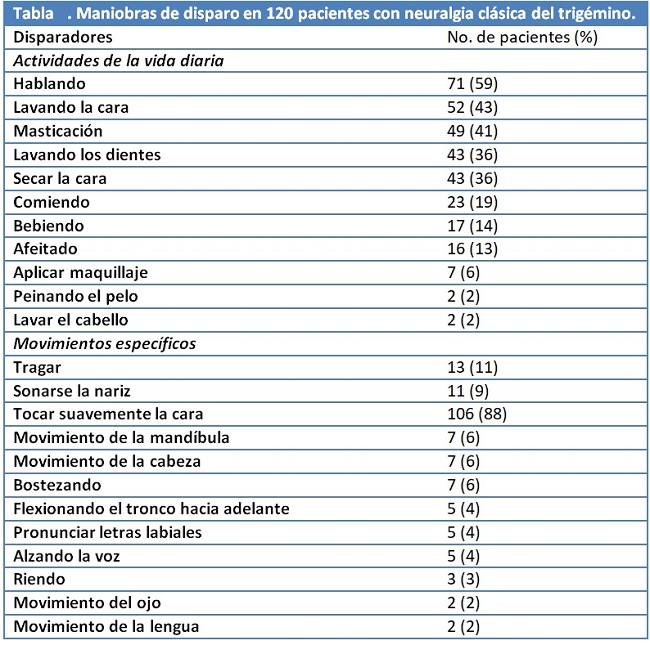
Las maniobras de activación específicas de una serie de pacientes se muestran en la siguiente tabla, y la distribución de las zonas de activación que provocan dolor se muestra en la figura anterior. Pocos pacientes informan que no hay desencadenantes.
El examen de la neuralgia del trigémino incluye la observación de la cara mientras el paciente está sentado y permanece completamente quieto. Con un paroxismo espontáneo de neuralgia del trigémino, el médico puede notar un parpadeo o un pequeño movimiento de la boca que el paciente desconoce.
Con menos frecuencia, durante un ataque paroxístico, puede ocurrir una contracción enérgica de los músculos faciales, llamada “tic convulsivo”. El examen sensorial de la cara por lo general es poco revelador en casos de neuralgia del trigémino, aunque algunos pacientes refieren áreas de hipoestesia leve.
Tipos y causas
Se han delineado tres tipos de neuralgia del trigémino: clásica, secundaria e idiopática. El tipo clásico, que es el más común, es causado por la compresión vascular intracraneal de la raíz del nervio trigémino, como se describe a continuación. El vaso responsable suele ser la arteria cerebelosa superior, que induce cambios morfológicos en la raíz del nervio trigémino adyacente.
La neuralgia secundaria del trigémino, que representa aproximadamente el 15% de los casos, es atribuible a una enfermedad neurológica identificable como la esclerosis múltiple o un tumor en el ángulo pontocerebeloso, que altera la zona de entrada de la raíz del nervio trigémino o comprime el nervio en su parte extracraneal.
La neuralgia idiopática del trigémino, en la que no se puede encontrar una causa aparente, representa aproximadamente el 10% de los casos.
Las características clínicas de la neuralgia del trigémino clásica y secundaria son similares, aunque los pacientes con neuralgia del trigémino secundaria suelen ser más jóvenes, más propensos a tener pérdida sensorial en una parte de la cara y es más probable que tengan dolor bilateral.
Dado que las tres formas de neuralgia del trigémino pueden ser clínicamente indistinguibles, es aconsejable realizar una resonancia magnética (RM) con gadolinio para descartar esclerosis múltiple y masas pontocerebelosas en el momento del diagnóstico inicial.
Un estudio reciente mostró variantes raras en genes que codifican canales iónicos dependientes de voltaje en pacientes con antecedentes familiares de neuralgia del trigémino clásica o idiopática, pero se desconoce la frecuencia e importancia clínica de este hallazgo.
Compresión neurovascular en la neuralgia clásica del trigémino
Durante las últimas décadas, la forma clásica de neuralgia del trigémino se ha revelado a través del trabajo de Jannetta et al, y se ha estudiado el potencial de curación mediante cirugía microvascular intracraneal.
Se considera que la fisiopatología es la compresión de la porción sensitiva del nervio trigémino, cerca de su zona de entrada en la protuberancia, por una pequeña rama adyacente de la arteria basilar, más a menudo la arteria cerebelosa superior. Sin embargo, el simple contacto entre el nervio y una estructura vascular no parece ser adecuado para causar o explicar el trastorno.
Para atribuir el trastorno a la compresión neurovascular, lo ideal sería demostrar que el vaso anómalo induce alteraciones anatómicas en la raíz del trigémino, como distorsión o atrofia. El hallazgo más característico en la operación es una pequeña arteria tortuosa o asa arterial que incide en la cara medial de la raíz del trigémino en su zona de entrada, provocando dislocación lateral, distorsión, aplanamiento o atrofia de la raíz del nervio.
La compresión neurovascular se puede ver con el uso de resonancia magnética y reconstrucción tridimensional. Las técnicas de imagen incluyen secuencias de resonancia magnética en T2 tridimensionales con examen detallado de los segmentos cisternal y cavernoso del nervio, angiografía por resonancia magnética tridimensional para la visualización de arterias y resonancia magnética con contraste de fase para mostrar las venas.
La descompresión vascular puede revertir estas anomalías en la zona de entrada de la raíz del trigémino, donde la porción sensitiva del nervio entra en la protuberancia.
Fisiopatología
En su entrada a la protuberancia, el nervio trigémino (como todos los nervios periféricos) pierde su vaina de mielina de las células de Schwann y es reemplazada por mielina central generada por oligodendroglia.
Esta zona de transición es vulnerable al daño y particularmente a la desmielinización. La compresión vascular es la causa habitual de desmielinización antes de que el nervio entre en la protuberancia y la esclerosis múltiple es la causa típica justo después de la entrada en la protuberancia. La desmielinización en estos sitios se ha demostrado en estudios neurofisiológicos, de neuroimagen e histológicos.
Cuando la vaina de mielina se vuelve lo suficientemente delgada como para permitir el paso transmembrana de iones en el axón subyacente, el axón no está equipado para bombear sodio rápidamente.
La despolarización resultante hace que el axón sea hiperexcitable, provocando una generación ectópica de impulsos con posdescargas de alta frecuencia (descargas que ocurren después de la terminación del estímulo) y diafonía entre fibras (llamada transmisión efáptica). La evidencia histológica indica que las fibras nerviosas más involucradas en la desmielinización son las fibras A-β (fibras grandes, no nociceptivas), que son las más susceptibles a la desmielinización por daño mecánico o esclerosis múltiple.
Se ha propuesto que las descargas de alta frecuencia que se originan en el sitio de desmielinización a lo largo de las aferentes primarias A-β son redirigidas por las neuronas del tronco encefálico para ser percibidas como dolor paroxístico.
Algunos investigadores han observado una excitabilidad excesiva o reducciones en el volumen de varias áreas cerebrales corticales y subcorticales en pacientes con neuralgia del trigémino, pero estos cambios son probablemente consecuencia de la adaptación a la estimulación crónica de estas regiones.
Neuralgia del trigémino con dolor continuo
El mecanismo subyacente al dolor continuo es diferente del mecanismo subyacente al dolor paroxístico, como sugiere el menor grado de alivio del dolor continuo, en comparación con el dolor paroxístico, después del tratamiento con bloqueadores de los canales de sodio o descompresión microvascular.
El vínculo fisiopatológico entre las dos entidades del dolor es incierto. Se ha planteado la hipótesis del daño progresivo de la raíz nerviosa y los mecanismos de sensibilización central. El dolor tipo ardiente, punzante o molestia probablemente esté mediado por el deterioro de las fibras C (axones sensoriales amielínicos que transmiten impulsos lentamente), como se muestra en otras condiciones de dolor neuropático.
La pérdida de fibras C en la raíz sensorial del trigémino puede causar una actividad espontánea anormal en las neuronas de segundo orden en el tallo cerebral. La noción anterior de que el dolor continuo se desarrolla como resultado de una neuralgia del trigémino de larga duración no está respaldada por datos más recientes.
Neuralgia secundaria del trigémino
En el 15% de los pacientes con ataques de dolor típicos, la neuralgia del trigémino es causada por esclerosis múltiple o por tumores benignos en el ángulo pontocerebeloso. El riesgo de neuralgia del trigémino se multiplica por 20 entre los pacientes con esclerosis múltiple, en comparación con la población general, con una prevalencia del 2 al 5% entre los pacientes con esclerosis múltiple.
En ocasiones, la neuralgia del trigémino se manifiesta como un síndrome clínicamente aislado en pacientes con esclerosis múltiple; la edad de inicio de la esclerosis múltiple es mayor en estos pacientes que en aquellos que no tienen neuralgia del trigémino.
Un estudio de neuroimagen ha mostrado una asociación entre la compresión neurovascular y la neuralgia del trigémino relacionada con la esclerosis múltiple, lo que sugiere que pueden coexistir y ser aditivas. Se desconoce la frecuencia de este mecanismo dual, pero tiene implicaciones para el tratamiento.
El tratamiento farmacológico del dolor de la neuralgia del trigémino en pacientes con esclerosis múltiple es un desafío debido a los efectos secundarios de los medicamentos, el empeoramiento de los síntomas de la esclerosis múltiple como la fatiga y la ataxia y la evidencia limitada de su efectividad en tales pacientes.
Las series de casos indican que los procedimientos quirúrgicos para reducir la compresión vascular tienden a ser menos efectivos que en pacientes con neuralgia del trigémino clásica.
Los tumores en el ángulo pontinocerebeloso que comprimen la raíz del nervio trigémino y causan neuralgia del trigémino incluyen neurinomas acústicos, meningiomas, quistes epidermoides y colesteatomas. Curiosamente, los neurinomas del trigémino (que son raros) no se han asociado con la neuralgia del trigémino.
En un análisis de datos de cuatro estudios que incluyeron a 243 pacientes con neuralgia del trigémino, los tumores fueron la causa en 20 pacientes (8%). La compresión del nervio trigémino por los tumores induce la desmielinización focal de la raíz del nervio trigémino, desencadenando la misma generación de descargas de alta frecuencia en axones desnudos que ocurre en la compresión vascular del nervio. Los tumores malignos infiltrantes también pueden causar degeneración axonal, lo que resulta en hipoestesia en regiones de la cara y dolor persistente.
Las neuropatías del trigémino debidas a traumatismos y enfermedades reumatológicas como el lupus eritematoso sistémico y la esclerodermia pueden manifestarse como dolor paroxístico que simula la neuralgia del trigémino, pero estas asociaciones son poco frecuentes.
Los traumatismos faciales, los procedimientos dentales o la cirugía maxilofacial pueden dañar las ramas del nervio trigémino, provocando un pinchazo paroxístico, similar a una descarga eléctrica o dolor ardiente. Sin embargo, los ataques de dolor tienen una duración más prolongada que los paroxismos de la neuralgia del trigémino, y la mayoría de los pacientes también describen un dolor intenso continuo sin zonas de activación sensoriales.
La neuropatía del trigémino idiopática aislada, una neuropatía benigna bilateral, simétrica, puramente sensorial, y la neuropatía motora sensorial de inicio facial, una enfermedad progresiva más grave, también pueden manifestarse inicialmente como dolor facial paroxístico unilateral.
Tratamiento
Tratamiento médico
Los agentes anticonvulsivos carbamazepina, en dosis de aproximadamente 200 a 1.200 mg por día, y oxcarbazepina (300 a 1.800 mg por día) se han considerado los tratamientos de primera elección para el control del dolor paroxístico en pacientes con neuralgia del trigémino, independientemente de la causa, con un control significativo del dolor en casi el 90% de los pacientes.
Se propone el efecto del tratamiento que estar relacionado con el bloqueo de canales de sodio dependientes de voltaje, lo que resulta en la estabilización de las membranas neuronales hiperexcitadas y la inhibición de la descarga repetitiva.
Sin embargo, la mejoría clínica a menudo se ve acompañada por efectos secundarios, que incluyen mareos, diplopía, ataxia y niveles elevados de aminotransferasas, los cuales pueden provocar la suspensión del tratamiento en el 23% de los pacientes.
La oxcarbazepina puede tener menos efectos secundarios que la carbamazepina, aunque puede suspenderse debido a una depresión excesiva del sistema nervioso central o hiponatremia relacionada con la dosis.
Las contraindicaciones para el uso de bloqueadores de los canales de sodio incluyen problemas de conducción cardíaca y reacciones alérgicas, con un alto grado de reactividad cruzada (40 a 80%) con fármacos antiepilépticos aromáticos.
La carbamazepina y la oxcarbazepina reducen las descargas de alta frecuencia que caracterizan los paroxismos similares a descargas eléctricas, pero el efecto de estos fármacos sobre el dolor continuo concomitante suele ser limitado.
La gabapentina, la pregabalina y los agentes antidepresivos, que han demostrado ser eficaces en el tratamiento de otras afecciones neuropáticas caracterizadas por dolor continuo, pueden probarse como agentes adicionales junto con la oxcarbazepina o la carbamazepina.
La experiencia clínica sugiere que la gabapentina puede tener un efecto menor sobre la neuralgia del trigémino que la carbamazepina y la oxcarbazepina, pero se asocia con una menor incidencia de eventos adversos y puede intentarse como monoterapia o como terapia complementaria, incluso en pacientes con esclerosis múltiple.
Aunque los procedimientos quirúrgicos son eficaces para reducir la gravedad y la frecuencia de los ataques de neuralgia del trigémino en pacientes elegidos adecuadamente, este tipo de cirugía generalmente se realiza solo si las dosis estándar de medicamentos no son suficientes para controlar los síntomas o si los efectos secundarios impiden su uso continuado.
Un grupo de intervenciones quirúrgicas, ahora utilizadas con poca frecuencia, implica el bloqueo periférico de las ramas del nervio trigémino al emerger de los huesos faciales mediante neurectomía, inyecciones de alcohol o inducción de lesiones por radiofrecuencia o criolesiones.
El propósito de estos procedimientos es producir un área de anestesia en la cara que corresponda a la distribución del nervio dañado. Sin embargo, el beneficio de tales tratamientos no ha sido respaldado adecuadamente por ensayos, y los procedimientos a menudo condujeron a anestesia dolorosa (dolor intenso en el área de la pérdida sensorial).
Un segundo grupo de intervenciones pretende dañar por vía percutánea el ganglio trigeminal en el cavum de Meckel o la salida de las ramas del ganglio en la base del cráneo por medio de termocoagulación por radiofrecuencia, destrucción química a través de la inyección de glicerol, o compresión mecánica a través de inflado del balón.
La termocoagulación por radiofrecuencia daña preferentemente las fibras dolorosas de pequeño diámetro. Para prevenir la desaferenciación de la córnea y la queratitis resultante, el electrodo se orienta para evitar dañar la primera división del nervio trigémino. La compresión con balón y la inyección de glicerol dañan preferentemente las fibras mielinizadas grandes.
El alivio del dolor es inmediato con estas técnicas. Los déficits sensoriales del trigémino suelen ser transitorios con la compresión con balón y la inyección de glicerol y son más graves y duraderos después de la termocoagulación por radiofrecuencia.
La generación de una lesión de la raíz del trigémino con un bisturí de rayos gamma es un procedimiento introducido más recientemente y está respaldado por varios estudios. En contraste con el alivio inmediato del dolor asociado con las lesiones del ganglio trigémino causadas por vía percutánea, el efecto analgésico de la radiocirugía estereotáctica con bisturí de rayos gamma tarda de 6 a 8 semanas en desarrollarse. Aproximadamente del 24 al 71% de los pacientes informan un alivio continuo del dolor de 1 a 2 años después de someterse al procedimiento, y del 33 al 56% informan un alivio continuo del dolor a los 4 a 5 años.
Se ha informado entumecimiento facial en el 16% de los pacientes, mientras que la anestesia dolorosa está prácticamente ausente. Un metaanálisis mostró que aproximadamente el 34% de los pacientes no experimentan alivio del dolor al año y requieren procedimientos repetidos.
Descompresión microvascular
La descompresión microvascular se ha convertido actualmente en el procedimiento quirúrgico de elección para la mayoría de los casos de neuralgia del trigémino que no responden a la medicación.
El neurocirujano identifica el vaso que está comprimiendo la raíz del nervio trigémino, lo mueve desde debajo del nervio hacia encima del nervio si es necesario (ver figura más abajo) y, por lo general, inserta una pequeña esponja para mantener la arteria pulsante separada de la raíz nerviosa.
En aproximadamente el 11% de los pacientes, el cirujano no encuentra compresión neurovascular o encuentra un contacto mínimo, sin compresión aparente del nervio. En estos casos, el cirujano generalmente inserta la esponja separadora de todos modos, aunque la tasa de falla es mayor que cuando se identifica una distorsión de la raíz nerviosa. Este problema subraya la ventaja de utilizar los criterios de resonancia magnética establecidos para identificar cambios morfológicos en la raíz del trigémino.
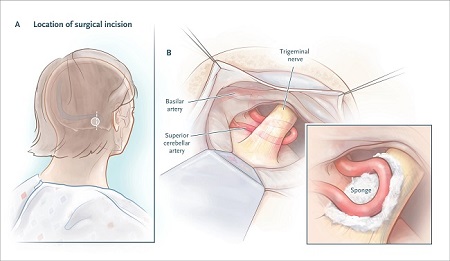
Descompresión microvascular.Los metanálisis han sugerido que la descompresión microvascular es la intervención quirúrgica más eficaz para la neuralgia clásica del trigémino. De 1 a 2 años después de someterse al procedimiento, del 68 al 88% de los pacientes experimentan alivio del dolor y del 61 al 80% tienen alivio del dolor a los 4 a 5 años.
La mortalidad media asociada a la cirugía es del 0,3%. Las fugas de líquido cefalorraquídeo se presentan en el 2,0% de los pacientes, los infartos o hematomas del tronco encefálico en el 0,6% y la meningitis en el 0,4%.
La pérdida sensorial en parte o en su totalidad de la distribución sensorial del nervio trigémino en la cara ocurre en 2.9% de los pacientes. La complicación a largo plazo más preocupante, aunque rara (incidencia, 1,8%), es la hipoacusia ipsilateral.
A los pacientes con esclerosis múltiple que tienen neuralgia del trigémino resistente a fármacos se les puede ofrecer descompresión microvascular, aunque la evidencia es insuficiente. Sin embargo, también se ha informado que tanto las lesiones percutáneas como las lesiones con bisturí de rayos gamma tienen buenos resultados en pacientes con esclerosis múltiple.
La neuralgia del trigémino, tradicionalmente llamada tic doloroso, es un trastorno de dolor neuropático crónico caracterizado por paroxismos espontáneos y provocados de dolor punzante o similar a una descarga eléctrica en una región de la cara. Se han atribuido al trastorno una mala calidad de vida y el suicidio en casos graves.
Características clínicas y diagnóstico
El diagnóstico de neuralgia del trigémino es clínico y se basa en tres criterios principales:
- Dolor restringido al territorio de una o más divisiones del nervio trigémino.
- Paroxismos de dolor que son repentinos, intensos y muy breves (de menos de 1 segundo a 2 minutos, pero generalmente unos pocos segundos) y se describen como un "shock" o una "sensación eléctrica".
- Dolor desencadenado por estímulos inocuos en la cara o territorio intraoral del trigémino.
El dolor de la neuralgia del trigémino afecta con mayor frecuencia la distribución de la segunda (maxilar) o tercer (mandibular) división del nervio trigémino, afectando el lado derecho de la cara con más frecuencia que el lado izquierdo.
La neuralgia bilateral del trigémino es poco común y debe suscitar preocupación por la posibilidad de neuralgia facial debida a una enfermedad neurológica subyacente o un trastorno no neurológico que afecta al cráneo.
La incidencia de neuralgia del trigémino es mayor entre las mujeres que entre los hombres y aumenta con la edad.Muchas formas de dolor facial se han combinado con la neuralgia del trigémino, pero es probable que sean entidades distintas, a veces incluidas en la categoría de "dolor facial atípico" o "neuropatía dolorosa del trigémino".
El tercio posterior del cuero cabelludo, el oído externo (a excepción del trago) y la piel que recubre el ángulo de la mandíbula no están inervados por el nervio trigémino y no son sitios de dolor debido a la neuralgia del trigémino (ver figura a continuación); el dolor en estas áreas sugiere un proceso diferente.

Territorios de inervación del nervio trigémino y distribución de la zona de activación.
La ubicación del dolor no siempre es concordante con el lugar del desencadenante sensorial. Por ejemplo, los estímulos en y alrededor del labio inferior pueden inducir dolor en la sien, o los desencadenantes sensoriales en las porciones laterales de la nariz pueden inducir un dolor similar a un choque que se irradia hacia la frente o el labio superior.
Las maniobras de activación específicas de una serie de pacientes se muestran en la siguiente tabla, y la distribución de las zonas de activación que provocan dolor se muestra en la figura anterior. Pocos pacientes informan que no hay desencadenantes.

El examen de la neuralgia del trigémino incluye la observación de la cara mientras el paciente está sentado y permanece completamente quieto. Con un paroxismo espontáneo de neuralgia del trigémino, el médico puede notar un parpadeo o un pequeño movimiento de la boca que el paciente desconoce.
Con menos frecuencia, durante un ataque paroxístico, puede ocurrir una contracción enérgica de los músculos faciales, llamada “tic convulsivo”. El examen sensorial de la cara por lo general es poco revelador en casos de neuralgia del trigémino, aunque algunos pacientes refieren áreas de hipoestesia leve.
Tipos y causas
Se han delineado tres tipos de neuralgia del trigémino: clásica, secundaria e idiopática. El tipo clásico, que es el más común, es causado por la compresión vascular intracraneal de la raíz del nervio trigémino, como se describe a continuación. El vaso responsable suele ser la arteria cerebelosa superior, que induce cambios morfológicos en la raíz del nervio trigémino adyacente.
La neuralgia secundaria del trigémino, que representa aproximadamente el 15% de los casos, es atribuible a una enfermedad neurológica identificable como la esclerosis múltiple o un tumor en el ángulo pontocerebeloso, que altera la zona de entrada de la raíz del nervio trigémino o comprime el nervio en su parte extracraneal.
La neuralgia idiopática del trigémino, en la que no se puede encontrar una causa aparente, representa aproximadamente el 10% de los casos.
Las características clínicas de la neuralgia del trigémino clásica y secundaria son similares, aunque los pacientes con neuralgia del trigémino secundaria suelen ser más jóvenes, más propensos a tener pérdida sensorial en una parte de la cara y es más probable que tengan dolor bilateral.
Dado que las tres formas de neuralgia del trigémino pueden ser clínicamente indistinguibles, es aconsejable realizar una resonancia magnética (RM) con gadolinio para descartar esclerosis múltiple y masas pontocerebelosas en el momento del diagnóstico inicial.
Un estudio reciente mostró variantes raras en genes que codifican canales iónicos dependientes de voltaje en pacientes con antecedentes familiares de neuralgia del trigémino clásica o idiopática, pero se desconoce la frecuencia e importancia clínica de este hallazgo.
Compresión neurovascular en la neuralgia clásica del trigémino
Durante las últimas décadas, la forma clásica de neuralgia del trigémino se ha revelado a través del trabajo de Jannetta et al, y se ha estudiado el potencial de curación mediante cirugía microvascular intracraneal.
Se considera que la fisiopatología es la compresión de la porción sensitiva del nervio trigémino, cerca de su zona de entrada en la protuberancia, por una pequeña rama adyacente de la arteria basilar, más a menudo la arteria cerebelosa superior. Sin embargo, el simple contacto entre el nervio y una estructura vascular no parece ser adecuado para causar o explicar el trastorno.
Para atribuir el trastorno a la compresión neurovascular, lo ideal sería demostrar que el vaso anómalo induce alteraciones anatómicas en la raíz del trigémino, como distorsión o atrofia. El hallazgo más característico en la operación es una pequeña arteria tortuosa o asa arterial que incide en la cara medial de la raíz del trigémino en su zona de entrada, provocando dislocación lateral, distorsión, aplanamiento o atrofia de la raíz del nervio.
La compresión neurovascular se puede ver con el uso de resonancia magnética y reconstrucción tridimensional. Las técnicas de imagen incluyen secuencias de resonancia magnética en T2 tridimensionales con examen detallado de los segmentos cisternal y cavernoso del nervio, angiografía por resonancia magnética tridimensional para la visualización de arterias y resonancia magnética con contraste de fase para mostrar las venas.
La descompresión vascular puede revertir estas anomalías en la zona de entrada de la raíz del trigémino, donde la porción sensitiva del nervio entra en la protuberancia.
Fisiopatología
En su entrada a la protuberancia, el nervio trigémino (como todos los nervios periféricos) pierde su vaina de mielina de las células de Schwann y es reemplazada por mielina central generada por oligodendroglia.
Esta zona de transición es vulnerable al daño y particularmente a la desmielinización. La compresión vascular es la causa habitual de desmielinización antes de que el nervio entre en la protuberancia y la esclerosis múltiple es la causa típica justo después de la entrada en la protuberancia. La desmielinización en estos sitios se ha demostrado en estudios neurofisiológicos, de neuroimagen e histológicos.
Cuando la vaina de mielina se vuelve lo suficientemente delgada como para permitir el paso transmembrana de iones en el axón subyacente, el axón no está equipado para bombear sodio rápidamente.
La despolarización resultante hace que el axón sea hiperexcitable, provocando una generación ectópica de impulsos con posdescargas de alta frecuencia (descargas que ocurren después de la terminación del estímulo) y diafonía entre fibras (llamada transmisión efáptica). La evidencia histológica indica que las fibras nerviosas más involucradas en la desmielinización son las fibras A-β (fibras grandes, no nociceptivas), que son las más susceptibles a la desmielinización por daño mecánico o esclerosis múltiple.
Se ha propuesto que las descargas de alta frecuencia que se originan en el sitio de desmielinización a lo largo de las aferentes primarias A-β son redirigidas por las neuronas del tronco encefálico para ser percibidas como dolor paroxístico.
Algunos investigadores han observado una excitabilidad excesiva o reducciones en el volumen de varias áreas cerebrales corticales y subcorticales en pacientes con neuralgia del trigémino, pero estos cambios son probablemente consecuencia de la adaptación a la estimulación crónica de estas regiones.
Neuralgia del trigémino con dolor continuo
Aunque el dolor facial paroxístico es el sello distintivo de la neuralgia del trigémino, del 24 al 49% de los pacientes refieren dolor continuo o prolongado entre los ataques paroxísticos.El dolor de fondo fluctuante, con una distribución que es consistente con la del dolor paroxístico, se describe como ardor, dolor pulsátil o molestia. La neuralgia del trigémino caracterizada por este síntoma, independientemente de la causa, ha sido previamente clasificada como neuralgia del trigémino tipo 2 o atípica y ahora se clasifica como la neuralgia del trigémino con dolor continuo concomitante.
El mecanismo subyacente al dolor continuo es diferente del mecanismo subyacente al dolor paroxístico, como sugiere el menor grado de alivio del dolor continuo, en comparación con el dolor paroxístico, después del tratamiento con bloqueadores de los canales de sodio o descompresión microvascular.
El vínculo fisiopatológico entre las dos entidades del dolor es incierto. Se ha planteado la hipótesis del daño progresivo de la raíz nerviosa y los mecanismos de sensibilización central. El dolor tipo ardiente, punzante o molestia probablemente esté mediado por el deterioro de las fibras C (axones sensoriales amielínicos que transmiten impulsos lentamente), como se muestra en otras condiciones de dolor neuropático.
La pérdida de fibras C en la raíz sensorial del trigémino puede causar una actividad espontánea anormal en las neuronas de segundo orden en el tallo cerebral. La noción anterior de que el dolor continuo se desarrolla como resultado de una neuralgia del trigémino de larga duración no está respaldada por datos más recientes.
Neuralgia secundaria del trigémino
En el 15% de los pacientes con ataques de dolor típicos, la neuralgia del trigémino es causada por esclerosis múltiple o por tumores benignos en el ángulo pontocerebeloso. El riesgo de neuralgia del trigémino se multiplica por 20 entre los pacientes con esclerosis múltiple, en comparación con la población general, con una prevalencia del 2 al 5% entre los pacientes con esclerosis múltiple.
En ocasiones, la neuralgia del trigémino se manifiesta como un síndrome clínicamente aislado en pacientes con esclerosis múltiple; la edad de inicio de la esclerosis múltiple es mayor en estos pacientes que en aquellos que no tienen neuralgia del trigémino.
Un estudio de neuroimagen ha mostrado una asociación entre la compresión neurovascular y la neuralgia del trigémino relacionada con la esclerosis múltiple, lo que sugiere que pueden coexistir y ser aditivas. Se desconoce la frecuencia de este mecanismo dual, pero tiene implicaciones para el tratamiento.
El tratamiento farmacológico del dolor de la neuralgia del trigémino en pacientes con esclerosis múltiple es un desafío debido a los efectos secundarios de los medicamentos, el empeoramiento de los síntomas de la esclerosis múltiple como la fatiga y la ataxia y la evidencia limitada de su efectividad en tales pacientes.
Las series de casos indican que los procedimientos quirúrgicos para reducir la compresión vascular tienden a ser menos efectivos que en pacientes con neuralgia del trigémino clásica.
Los tumores en el ángulo pontinocerebeloso que comprimen la raíz del nervio trigémino y causan neuralgia del trigémino incluyen neurinomas acústicos, meningiomas, quistes epidermoides y colesteatomas. Curiosamente, los neurinomas del trigémino (que son raros) no se han asociado con la neuralgia del trigémino.
En un análisis de datos de cuatro estudios que incluyeron a 243 pacientes con neuralgia del trigémino, los tumores fueron la causa en 20 pacientes (8%). La compresión del nervio trigémino por los tumores induce la desmielinización focal de la raíz del nervio trigémino, desencadenando la misma generación de descargas de alta frecuencia en axones desnudos que ocurre en la compresión vascular del nervio. Los tumores malignos infiltrantes también pueden causar degeneración axonal, lo que resulta en hipoestesia en regiones de la cara y dolor persistente.
Las neuropatías del trigémino debidas a traumatismos y enfermedades reumatológicas como el lupus eritematoso sistémico y la esclerodermia pueden manifestarse como dolor paroxístico que simula la neuralgia del trigémino, pero estas asociaciones son poco frecuentes.
Los traumatismos faciales, los procedimientos dentales o la cirugía maxilofacial pueden dañar las ramas del nervio trigémino, provocando un pinchazo paroxístico, similar a una descarga eléctrica o dolor ardiente. Sin embargo, los ataques de dolor tienen una duración más prolongada que los paroxismos de la neuralgia del trigémino, y la mayoría de los pacientes también describen un dolor intenso continuo sin zonas de activación sensoriales.
La neuropatía del trigémino idiopática aislada, una neuropatía benigna bilateral, simétrica, puramente sensorial, y la neuropatía motora sensorial de inicio facial, una enfermedad progresiva más grave, también pueden manifestarse inicialmente como dolor facial paroxístico unilateral.
La prueba del reflejo corneal se ha utilizado como técnica neurofisiológica para detectar el daño del nervio trigémino.Esta prueba de diagnóstico es útil en pacientes que no pueden someterse a una resonancia magnética o para detectar desmielinización y neuropatías que imitan la neuralgia del trigémino.
Tratamiento
Tratamiento médico
Los agentes anticonvulsivos carbamazepina, en dosis de aproximadamente 200 a 1.200 mg por día, y oxcarbazepina (300 a 1.800 mg por día) se han considerado los tratamientos de primera elección para el control del dolor paroxístico en pacientes con neuralgia del trigémino, independientemente de la causa, con un control significativo del dolor en casi el 90% de los pacientes.
Se propone el efecto del tratamiento que estar relacionado con el bloqueo de canales de sodio dependientes de voltaje, lo que resulta en la estabilización de las membranas neuronales hiperexcitadas y la inhibición de la descarga repetitiva.
Sin embargo, la mejoría clínica a menudo se ve acompañada por efectos secundarios, que incluyen mareos, diplopía, ataxia y niveles elevados de aminotransferasas, los cuales pueden provocar la suspensión del tratamiento en el 23% de los pacientes.
La oxcarbazepina puede tener menos efectos secundarios que la carbamazepina, aunque puede suspenderse debido a una depresión excesiva del sistema nervioso central o hiponatremia relacionada con la dosis.
Las contraindicaciones para el uso de bloqueadores de los canales de sodio incluyen problemas de conducción cardíaca y reacciones alérgicas, con un alto grado de reactividad cruzada (40 a 80%) con fármacos antiepilépticos aromáticos.
La carbamazepina y la oxcarbazepina reducen las descargas de alta frecuencia que caracterizan los paroxismos similares a descargas eléctricas, pero el efecto de estos fármacos sobre el dolor continuo concomitante suele ser limitado.
La gabapentina, la pregabalina y los agentes antidepresivos, que han demostrado ser eficaces en el tratamiento de otras afecciones neuropáticas caracterizadas por dolor continuo, pueden probarse como agentes adicionales junto con la oxcarbazepina o la carbamazepina.
La experiencia clínica sugiere que la gabapentina puede tener un efecto menor sobre la neuralgia del trigémino que la carbamazepina y la oxcarbazepina, pero se asocia con una menor incidencia de eventos adversos y puede intentarse como monoterapia o como terapia complementaria, incluso en pacientes con esclerosis múltiple.
Si el tratamiento médico es ineficaz o está asociado con efectos secundarios inaceptables, se puede considerar la descompresión quirúrgica del nervio trigémino.Procedimientos quirúrgicos locales
Aunque los procedimientos quirúrgicos son eficaces para reducir la gravedad y la frecuencia de los ataques de neuralgia del trigémino en pacientes elegidos adecuadamente, este tipo de cirugía generalmente se realiza solo si las dosis estándar de medicamentos no son suficientes para controlar los síntomas o si los efectos secundarios impiden su uso continuado.
Un grupo de intervenciones quirúrgicas, ahora utilizadas con poca frecuencia, implica el bloqueo periférico de las ramas del nervio trigémino al emerger de los huesos faciales mediante neurectomía, inyecciones de alcohol o inducción de lesiones por radiofrecuencia o criolesiones.
El propósito de estos procedimientos es producir un área de anestesia en la cara que corresponda a la distribución del nervio dañado. Sin embargo, el beneficio de tales tratamientos no ha sido respaldado adecuadamente por ensayos, y los procedimientos a menudo condujeron a anestesia dolorosa (dolor intenso en el área de la pérdida sensorial).
Un segundo grupo de intervenciones pretende dañar por vía percutánea el ganglio trigeminal en el cavum de Meckel o la salida de las ramas del ganglio en la base del cráneo por medio de termocoagulación por radiofrecuencia, destrucción química a través de la inyección de glicerol, o compresión mecánica a través de inflado del balón.
La termocoagulación por radiofrecuencia daña preferentemente las fibras dolorosas de pequeño diámetro. Para prevenir la desaferenciación de la córnea y la queratitis resultante, el electrodo se orienta para evitar dañar la primera división del nervio trigémino. La compresión con balón y la inyección de glicerol dañan preferentemente las fibras mielinizadas grandes.
El alivio del dolor es inmediato con estas técnicas. Los déficits sensoriales del trigémino suelen ser transitorios con la compresión con balón y la inyección de glicerol y son más graves y duraderos después de la termocoagulación por radiofrecuencia.
La generación de una lesión de la raíz del trigémino con un bisturí de rayos gamma es un procedimiento introducido más recientemente y está respaldado por varios estudios. En contraste con el alivio inmediato del dolor asociado con las lesiones del ganglio trigémino causadas por vía percutánea, el efecto analgésico de la radiocirugía estereotáctica con bisturí de rayos gamma tarda de 6 a 8 semanas en desarrollarse. Aproximadamente del 24 al 71% de los pacientes informan un alivio continuo del dolor de 1 a 2 años después de someterse al procedimiento, y del 33 al 56% informan un alivio continuo del dolor a los 4 a 5 años.
Se ha informado entumecimiento facial en el 16% de los pacientes, mientras que la anestesia dolorosa está prácticamente ausente. Un metaanálisis mostró que aproximadamente el 34% de los pacientes no experimentan alivio del dolor al año y requieren procedimientos repetidos.
Descompresión microvascular
La descompresión microvascular se ha convertido actualmente en el procedimiento quirúrgico de elección para la mayoría de los casos de neuralgia del trigémino que no responden a la medicación.
El neurocirujano identifica el vaso que está comprimiendo la raíz del nervio trigémino, lo mueve desde debajo del nervio hacia encima del nervio si es necesario (ver figura más abajo) y, por lo general, inserta una pequeña esponja para mantener la arteria pulsante separada de la raíz nerviosa.
En aproximadamente el 11% de los pacientes, el cirujano no encuentra compresión neurovascular o encuentra un contacto mínimo, sin compresión aparente del nervio. En estos casos, el cirujano generalmente inserta la esponja separadora de todos modos, aunque la tasa de falla es mayor que cuando se identifica una distorsión de la raíz nerviosa. Este problema subraya la ventaja de utilizar los criterios de resonancia magnética establecidos para identificar cambios morfológicos en la raíz del trigémino.

Descompresión microvascular.
La mortalidad media asociada a la cirugía es del 0,3%. Las fugas de líquido cefalorraquídeo se presentan en el 2,0% de los pacientes, los infartos o hematomas del tronco encefálico en el 0,6% y la meningitis en el 0,4%.
La pérdida sensorial en parte o en su totalidad de la distribución sensorial del nervio trigémino en la cara ocurre en 2.9% de los pacientes. La complicación a largo plazo más preocupante, aunque rara (incidencia, 1,8%), es la hipoacusia ipsilateral.
A los pacientes con esclerosis múltiple que tienen neuralgia del trigémino resistente a fármacos se les puede ofrecer descompresión microvascular, aunque la evidencia es insuficiente. Sin embargo, también se ha informado que tanto las lesiones percutáneas como las lesiones con bisturí de rayos gamma tienen buenos resultados en pacientes con esclerosis múltiple.
Conclusiones
|





















.png)










No hay comentarios:
Publicar un comentario