
Cerebro primero versus cuerpo primero | 02 SEP 20
Enfermedad de Parkinson, ¿hay dos variantes?
Enfermedad de Parkinson de cerebro primero versus cuerpo primero: un estudio de casos y controles de imágenes multimodales
Autor/a: Jacob Horsager, Katrine B Andersen, Karoline Knudsen, Casper Skjærbæk, et al. Fuente: Brain, awaa238, https://doi.org/10.1093/brain/awaa238 Brain-first versus body-first Parkinson’s disease: a multimodal imaging case-control study
La enfermedad de Parkinson se caracteriza por la presencia de agregados de α-sinucleína intraneuronales anormales, que pueden propagarse de una célula a otra de manera similar a un prión. Sin embargo, sigue siendo incierto dónde se originan los agregados iniciales de α-sinucleína.
Hemos planteado la hipótesis de que la enfermedad de Parkinson comprende dos subtipos.
Utilizando imágenes multimodales, probamos la hipótesis cuantificando la disfunción neuronal en estructuras correspondientes a las etapas I, II y III de Braak en tres grupos distintos de pacientes. Incluimos 37 pacientes consecutivos de novo con enfermedad de Parkinson en este estudio PET de casos y controles.
Los pacientes con enfermedad de Parkinson se dividieron en 24 casos RBD negativos (PDRBD−) y 13 casos RBD positivos (PDRBD +) y un grupo comparador de 22 pacientes iRBD.
Utilizamos PET / TC con 11C-donepezilo para evaluar la inervación colinérgica (parasimpática), gammagrafía con 123I-metayodobencilguanidina (MIBG) para medir la inervación simpática cardíaca, resonancia magnética sensible a neuromelanina para medir la integridad de las neuronas pigmentadas del locus coeruleus y 18F-dihidroxifenOpila PET para evaluar la capacidad de almacenamiento de dopamina putaminal.
El volumen del colon y los tiempos de tránsito se evaluaron con tomografías computarizadas y marcadores radiopacos. Los datos de imágenes de los tres grupos se interrogaron con ANOVA y pruebas de Kruskal-Wallis corregidas para múltiples comparaciones.
Los grupos PDRBD− y PDRBD + mostraron reducciones marcadas similares en la captación putaminal específica de FDOPA, mientras que dos tercios de los pacientes con iRBD tenían exploraciones normales (P <10-13, ANOVA).
En comparación con los pacientes con PDRBD−, los pacientes con PDRBD + e iRBD mostraron una reducción de las relaciones medias de MIBG corazón: mediastino (P <10−5, ANOVA) y valores estándar de captación de 11C-donepezil en el colon (P = 0,008, ANOVA).
El grupo PDRBD + mostró una tendencia hacia una proporción media de locus coeruleus: protuberancia de la resonancia magnética reducida en comparación con PDRBD− (P = 0,07, prueba t).
En comparación con los otros grupos, el grupo PDRBD + también tenía volúmenes de colon agrandados (P <0,001, ANOVA) y tiempos de tránsito colónico retrasados (P = 0,01, Kruskal-Wallis).
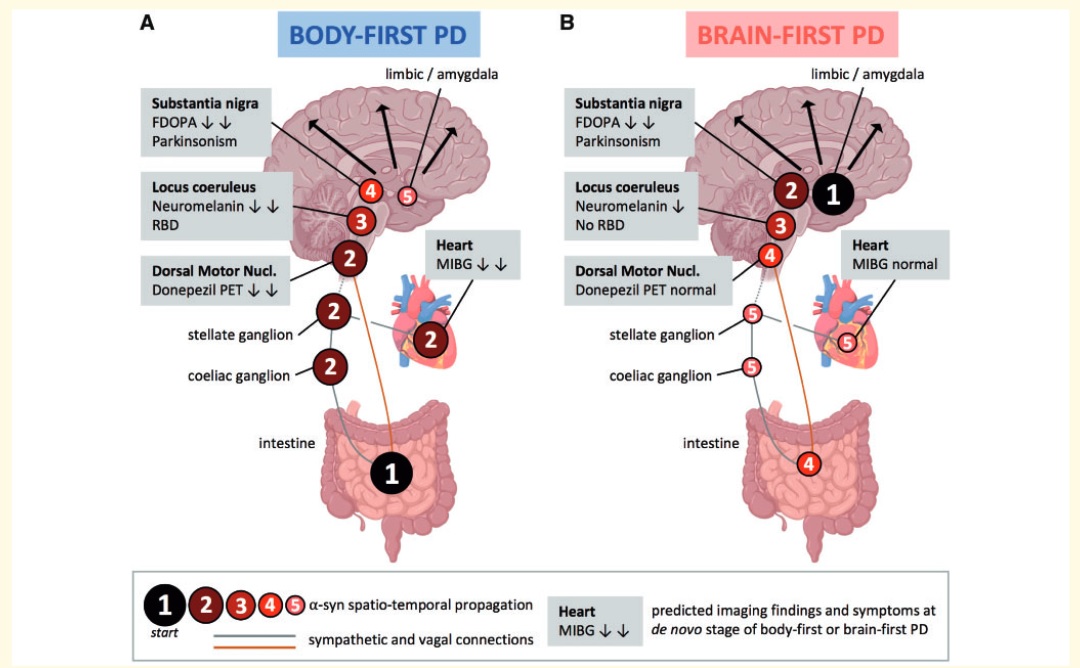
Los datos combinados de iRBD y PDRBD + del paciente fueron compatibles con una trayectoria de cuerpo primero, caracterizada por la pérdida inicial de la señal de MIBG cardíaca y la señal de donepezil colónico 11C seguida de la pérdida de captación de FDOPA putaminal.
Por el contrario, los datos de PDRBD− fueron compatibles con una trayectoria de cerebro primero, caracterizada por la pérdida primaria de la captación de FDOPA putaminal seguida de una pérdida secundaria de la señal de MIBG cardíaca y la señal de 11C-donepezilo.
 En conclusión, hemos demostrado que los pacientes prodrómicos y pacientes de novo con enfermedad de Parkinson pueden clasificarse mediante imágenes multimodales en grupos distintos, que son compatibles con un subtipo de enfermedad de Parkinson de tipo cerebro primero y cuerpo primero.
En conclusión, hemos demostrado que los pacientes prodrómicos y pacientes de novo con enfermedad de Parkinson pueden clasificarse mediante imágenes multimodales en grupos distintos, que son compatibles con un subtipo de enfermedad de Parkinson de tipo cerebro primero y cuerpo primero.
La presencia de RBD en la fase premotora es un marcador del tipo de cuerpo primero, probablemente un reflejo de patología de la a-sinucleína ascendente que alcanza la protuberancia antes de la sustancia negra. Es crucial que estos hallazgos sean replicados por investigadores independientes.
También será importante incluir otros tipos de pacientes prodrómicos con enfermedad de Parkinson, incluidos los portadores de mutaciones y los casos prodrómicos negativos para RBD, para estudiar qué tan cerca se alinean estos grupos de pacientes con las trayectorias del cerebro y el cuerpo primero.
Finalmente, ahora se necesita más investigación. para descubrir los factores etiológicos subyacentes a los subtipos. El eje cerebral intestinal y la microbiota se encuentran actualmente en un estudio intensivo. Sin embargo, parece probable que tales factores puedan ser principalmente causantes del tipo de cuerpo primero, pero tal vez sean irrelevantes para el subtipo de cerebro primero. Dichos descubrimientos serán fundamentales para el desarrollo de terapias específicas de subtipo para tratar y eventualmente prevenir la enfermedad de Parkinson.
Hemos planteado la hipótesis de que la enfermedad de Parkinson comprende dos subtipos.
- Un tipo de cerebro primero (de arriba hacia abajo), donde la patología de la α-sinucleína surge inicialmente en el cerebro con una extensión secundaria al sistema nervioso autónomo periférico.
- Un tipo de cuerpo primero (de abajo hacia arriba), donde la patología se origina en el sistema nervioso autónomo entérico o periférico y luego se disemina al cerebro.
Utilizando imágenes multimodales, probamos la hipótesis cuantificando la disfunción neuronal en estructuras correspondientes a las etapas I, II y III de Braak en tres grupos distintos de pacientes. Incluimos 37 pacientes consecutivos de novo con enfermedad de Parkinson en este estudio PET de casos y controles.
Los pacientes con enfermedad de Parkinson se dividieron en 24 casos RBD negativos (PDRBD−) y 13 casos RBD positivos (PDRBD +) y un grupo comparador de 22 pacientes iRBD.
Utilizamos PET / TC con 11C-donepezilo para evaluar la inervación colinérgica (parasimpática), gammagrafía con 123I-metayodobencilguanidina (MIBG) para medir la inervación simpática cardíaca, resonancia magnética sensible a neuromelanina para medir la integridad de las neuronas pigmentadas del locus coeruleus y 18F-dihidroxifenOpila PET para evaluar la capacidad de almacenamiento de dopamina putaminal.
El volumen del colon y los tiempos de tránsito se evaluaron con tomografías computarizadas y marcadores radiopacos. Los datos de imágenes de los tres grupos se interrogaron con ANOVA y pruebas de Kruskal-Wallis corregidas para múltiples comparaciones.
Los grupos PDRBD− y PDRBD + mostraron reducciones marcadas similares en la captación putaminal específica de FDOPA, mientras que dos tercios de los pacientes con iRBD tenían exploraciones normales (P <10-13, ANOVA).
En comparación con los pacientes con PDRBD−, los pacientes con PDRBD + e iRBD mostraron una reducción de las relaciones medias de MIBG corazón: mediastino (P <10−5, ANOVA) y valores estándar de captación de 11C-donepezil en el colon (P = 0,008, ANOVA).
El grupo PDRBD + mostró una tendencia hacia una proporción media de locus coeruleus: protuberancia de la resonancia magnética reducida en comparación con PDRBD− (P = 0,07, prueba t).
En comparación con los otros grupos, el grupo PDRBD + también tenía volúmenes de colon agrandados (P <0,001, ANOVA) y tiempos de tránsito colónico retrasados (P = 0,01, Kruskal-Wallis).
Los datos combinados de iRBD y PDRBD + del paciente fueron compatibles con una trayectoria de cuerpo primero, caracterizada por la pérdida inicial de la señal de MIBG cardíaca y la señal de donepezil colónico 11C seguida de la pérdida de captación de FDOPA putaminal.
Por el contrario, los datos de PDRBD− fueron compatibles con una trayectoria de cerebro primero, caracterizada por la pérdida primaria de la captación de FDOPA putaminal seguida de una pérdida secundaria de la señal de MIBG cardíaca y la señal de 11C-donepezilo.
Estos hallazgos apoyan la existencia de subtipos de la enfermedad de Parkinson de tipo cerebro primero y cuerpo primero.

La presencia de RBD en la fase premotora es un marcador del tipo de cuerpo primero, probablemente un reflejo de patología de la a-sinucleína ascendente que alcanza la protuberancia antes de la sustancia negra. Es crucial que estos hallazgos sean replicados por investigadores independientes.
También será importante incluir otros tipos de pacientes prodrómicos con enfermedad de Parkinson, incluidos los portadores de mutaciones y los casos prodrómicos negativos para RBD, para estudiar qué tan cerca se alinean estos grupos de pacientes con las trayectorias del cerebro y el cuerpo primero.
Finalmente, ahora se necesita más investigación. para descubrir los factores etiológicos subyacentes a los subtipos. El eje cerebral intestinal y la microbiota se encuentran actualmente en un estudio intensivo. Sin embargo, parece probable que tales factores puedan ser principalmente causantes del tipo de cuerpo primero, pero tal vez sean irrelevantes para el subtipo de cerebro primero. Dichos descubrimientos serán fundamentales para el desarrollo de terapias específicas de subtipo para tratar y eventualmente prevenir la enfermedad de Parkinson.





















.png)










No hay comentarios:
Publicar un comentario