
La resistencia a la insulina puede afectar a la regeneración hepática
Un nuevo estudio publicado en PLOS Biology desvela que la resistencia a la insulina podría favorecer la cicatrización del tejido hepático por encima de la regeneración. El trabajo abre nuevos enfoques en el campo de la medicina regenerativa del hígado.
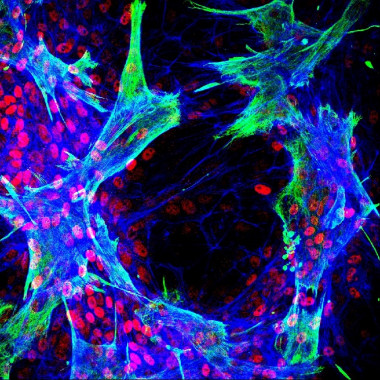
Imagen de inmunofluorescencia que muestra células estrelladas hepáticas primarias humanas que interactúan con células progenitoras hepáticas bipotentes in vitro. Los cultivos se marcaron utilizando anticuerpos contra vimentina (verde), HNF4a (rojo) y se trataron con faloidina (azul). El estudio mostró que la diferenciación de las células progenitoras se localizó en los sitios de contacto entre los dos tipos de células. / Luke Noon
Científicos del Centro de Investigación Príncipe Felipe (CIPF) y del Centro de Investigación Biomédica en Red de Diabetes y Enfermedades Metabólicas Asociadas (CIBERDEM), liderados por Luke Noon, han demostrado cómo la insulina tiene un papel clave en el proceso de reparación del hígado durante el daño crónico.
Según el nuevo estudio, publicado en PLOS Biology, la resistencia a la insulina –una afección muy común y estrechamente asociada con la enfermedad metabólica y la diabetes mellitus de tipo 2–, reduciría la habilidad de las células madre para responder ante el daño y generar nuevas células que permitan la reparación del tejido hepático.
Los pacientes con enfermedad metabólica son más susceptibles al daño hepático porque son incapaces de regenerar correctamente el hígado
“Los pacientes con enfermedad metabólica son más susceptibles al daño hepático porque son incapaces de regenerar correctamente el hígado” explica Noon, investigador Ramón y Cajal.
“El estudio respalda, por tanto, la prospección de que el desarrollo de patología hepática en pacientes con enfermedad metabólica podría verse impulsado por un fallo en la comunicación entre diferentes tipos celulares implicados en la respuesta regenerativa”, añade.
Los datos del estudio demuestran que la pérdida de funcionalidad de las células madre se desencadena por una disminución de los niveles de FGF7, una molécula de señalización producida por las células del tejido cicatrizante que rodean a las células madre. Después del daño, FGF7 actúa como una ‘señal de reparación’ enviada por las células del tejido cicatrizante y recibida por las células madre ayudando a dirigir la respuesta regenerativa.
‘Señales’ para reparar el hígado
El trabajo revela que, en el caso de los hígados de ratón resistentes a la insulina, el tejido cicatrizante no solo produce menos FGF7, sino que además la sensibilidad a FGF7 de las células madre es menor, lo que impide una correcta comunicación entre estos dos grupos de células tan esenciales para la maquinaria de reparación del hígado.
En concordancia con los resultados obtenidos a partir de ratones con resistencia a la insulina, la eliminación de un gen esencial para la señalización de insulina también redujo en las células humanas del tejido cicatrizante del hígado los niveles de FGF7 y provocó, en células madre humanas del hígado, una pérdida de su sensibilidad por FGF7 reduciendo su habilidad para generar tejido sano y cicatrizar.
Esto sugiere que la resistencia a la insulina podría favorecer la cicatrización del tejido por encima de la regeneración de este y que coincide con la creciente incidencia de cicatrización/fibrosis hepática en pacientes con enfermedad metabólica.
Para Noon, el modelo “ayuda a explicar los vínculos ya establecidos entre la resistencia a la insulina y la enfermedad hepática crónica a la vez que remarca el potencial de futuras intervenciones terapéuticas usando FGF7 para promover la reparación del hígado”.
Referencia bibliográfica:
Fátima Manzano-Núñez, María José Arámbul-Anthony, Amparo Galán Albiñana, Aranzazu Leal Tassias, Carlos Acosta Umanzor, Irene Borreda Gascó, Antonio Herrera, Jerónimo Forteza Vila, Deborah J. Burks, Luke A. Noon. Insulin resistance disrupts epithelial repair and niche-progenitor Fgf signaling during chronic liver injury. PLoS Biol 17 (1): e2006972.https://doi.org/10.1371/journal.pbio.2006972






















.png)










No hay comentarios:
Publicar un comentario