
Un fenómeno poco considerado y con graves consecuencias | 13 MAY 19
Hipoglucemia, enfermedad CV y mortalidad en diabetes
Epidemiología, patogénesis, tratamiento. Hipótesis actuales sobre su asociación

Autor: Vol 7,Issue 5, May 2019 Lancet Diabetes Endocrinol 2019
Página 1
| Introducción |
Se asocia a varias consecuencias vitales negativas, desde la interrupción de las actividades diarias hasta problemas psicosociales, tanto de los pacientes como de sus familiares.
A partir del descubrimiento de la insulina, se reconoce la posibilidad de que la hipoglucemia podría aumentar directamente la mortalidad.La lesión cerebral fatal debida a la neuroglucopenia severa es bastante rara, pero tras la interrupción anticipada del estudio ACORD (Control Cardiovascular Risk in Diabetes) debido a un aumento de la mortalidad de los participantes tratados intensivamente, ha habido un gran interés acerca de la asociación entre la hipoglucemia y los eventos cardiovasculares fatales.
El aumento de la mortalidad en el ensayo ACCORD provocó una considerable controversia con respecto a la causa subyacente.
| Las consecuencias cardiovasculares negativas de la hipoglucemia podrían explicar por qué el control glucémico intensivo no ha disminuido el riesgo de eventos de enfermedad cardiovascular en los ensayos clínicos. |
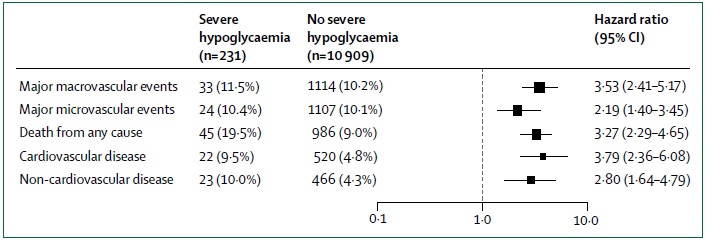
Asociación de hipoglucemia grave con el riesgo de un resultado clínico adverso o muerte
| Hipoglucemia y mortalidad |
Este informe podría haber subestimado el número de muertes por hipoglucemia, ya que las muertes causadas por infarto de miocardio y otras causas que podrían haber resultado de las arritmias cardíacas inducidas por la hipoglucemia fueron incluidas en categorías separadas.
Estudios noruegos más recientes han registrado una mayor prevalencia de muertes directas por hipoglucemia, en más del 8% de las personas con diabetes tipo 1 <56 años. Aunque este hallazgo podría reflejar una mayor precisión en la identificación de la causa de la muerte, otra explicación es que representa un aumento de la frecuencia de hipoglucemias y de la mortalidad asociada.
| Epidemiología |
El resultado del análisis observacional sugiere que un enfoque más intensivotuvo el potencial de prevenir los eventos macrovasculares. De hecho, el seguimiento extendido a 10 años luego de finalizado el ensayo mostró reducciones significativas de las tasas de infarto de miocardio y de mortalidad cardiovascular.
Tres ensayos clínicos aleatorizados posteriores probaron la hipótesis comparando el efecto del control glucémico menos intensivo con el control más intensivo, en individuos con diabetes tipo 2 establecida, sobre el aumento del riesgo cardiovascular, pero ninguno de los tres ensayos mostró reducciones significativas de los eventos cardiovasculares o de la mortalidad. De hecho, en uno de ellos, el ensayo ACCORD, la mortalidad aumentó.
Aunque existen otras causas potenciales de aumento de la mortalidad, como el aumento de peso, el uso de ciertos medicamentos, es digno de mención que en comparación con el ensayo ADVANCE (Action in Diabetes and Vascular Disease: Preterax and Diamicron MR Controlled Evaluation) que no mostró un aumento en la mortalidad, la frecuencia de hipoglucemia grave en el ACCORD fue 4-5 veces mayor.
Los tres estudios mostraron una asociación significativa entre la hipoglucemia grave y la mortalidad, aunque el Veteran’s Affairs Diabetes Trial (VADT) no fue muy potente al respecto.
En los ensayos VADT y ADVANCE, la hipoglucemia grave predijo la mortalidad alejada del episodio de hipoglucemia; en el ADVANCE, el tiempo medio desde la hipoglucemia grave hasta la muerte fue de 1,05 años.
La diferente duración de la diabetes entre estos estudios y el UKPDS podría ser importante para explicar sus diferentes resultados, ya que el UKPDS estudió a los diabéticos recién diagnosticados, mientras que los 3 ensayos más recientes reclutaron pacientes con diabetes con riesgo cardiovascular.
Aún se desconoce si la asociación en estos ensayos posteriores se debe a factores de confusión. Se ha argumentado que la confusión podría explicar la asociación entre la hipoglucemia y la mortalidad. Por ejemplo que las comorbilidades como la enfermedad renal o hepática, la malignidad, la pérdida de peso o el deterioro cognitivo confieren mayor riesgo de hipoglucemia y de eventos cardiovasculares.
Zoungas et al. sostienen que al menos parte de la mortalidad que en el ADVANCE es atribuida a la asociación con la gravedad de la hipoglucemia, es producto de la confusión. Esta conclusión surgió por el mayor cociente de riesgo de eventos no cardiovasculares en participantes que experimentaron hipoglucemia grave en comparación con aquellos que no tuvieron hipoglucemia.
Se especuló que los eventos de enfermedades respiratorias o gastrointestinales fueron los de menor probabilidad de haber sido ocasionados por hipoglucemias. Un grupo de nuevos estudios parra dilucidar esta cuestión ha incluido a decenas de miles de diabéticos tipo 1 o 2 de diferentes regiones del mundo y diferentes entornos de salud y han mostrado casi 1, 5-6 veces mayor riesgo de eventos cardiovasculares y mortalidad en los participantes con hipoglucemia, en comparación con los que no tuvieron hipoglucemia.
Este aumento del riesgo parece ser compartido por personas con ambos tipos de diabetes (DBT 1 y 2), aunque la magnitud del riesgo varía con el tipo de diabetes, los antecedentes de riesgo cardiovascular, las comorbilidades, la gravedad de la hipoglucemia, el momento del evento hipoglucémico, la duración del seguimiento y el nivel de ajuste por posibles factores de confusión.
La asociación no se limita a la hipoglucemia inducida por insulina, también se ha encontrado una asociación similar entre la hipoglucemia inducida por sulfonilureas. El análisis post-hoc adicional en otros ensayos con resultados cardiovasculares también ha planteado la probable contribución de la confusión como una explicación de la asociación.
La naturaleza observacional de muchos de los análisis y la incapacidad para capturar todos los episodios de hipoglucemia (particularmente los más leves o asintomáticos que podrían contribuir a los eventos cardiovasculares), han hecho difícil confirmar o refutar la causalidad, particularmente en relación con los eventos cardiovasculares.
Sin embargo, los resultados de algunos estudios han demostrado una asociación entre los eventos cardiovasculares (particularmente el infarto de miocardio) y la hipoglucemia. En cuanto a la asociación entre hipoglucemia e ictus, la evidencia parece menos consistente.
| En la mayoría de los estudios, la hipoglucemia grave se define como episodios que, para su recuperación, requieren la asistencia de otra persona. |
Si el control intensivo de la diabetes aumenta la tasa de episodios de hipoglucemias graves, cuando la hipoglucemia grave ocurre en personas frágiles y con comorbilidades que son más propensas a morir, podría ser considerada un marcador de riesgo de mortalidad.
Alternativamente, la hipoglucemia podría considerarse un factor de riesgo, en particular si los episodios son repetidos y no necesariamente graves, pues activa las respuestas fisiológicas que aceleran la actividad de la enfermedad cardiovascular.
Se hace notar que por razones éticas y prácticas no es posible realizar un estudio definitivo para probar la causalidad de la hipoglucemia grave para inducir deliberadamente episodios hipoglucémicos en un grupo y no en otro, y comparar la mortalidad de ambos.
Sin embargo, la conclusión de que existe una asociación causal entre la a hipoglucemia y los eventos cardiovasculares son apoyados por 2 revisiones sistemáticas, que utilizaron la técnica estadística de análisis de sesgos en metaanálisis de grandes números de participantes, en estudios observacionales.
Los autores de estas revisiones concluyeron que las comorbilidades graves por sí solas no pueden explicar la asociación, porque la prevalencia de la comorbilidad habría tenido que ser mucho más elevada de lo que era para dar cuenta de la asociación.
Por otra parte, Yeh y col. reportaron una relación dosis-respuesta (mayor asociación de la hipoglucemia grava que los episodios menos graves). Los autores también destacaron los diversos mecanismos fisiopatológicos plausibles que podrían contribuir a incrementar los eventos cardiovasculares.
Un estudio de 2018 apoya la hipótesis de que la hipoglucemia podría oponerse a los beneficios del control glucémico estricto, y que, de hecho, es un factor de riesgo de enfermedad cardiovascular.Un análisis de meta-regresión mostró que la reducción de la hemoglobina glicosilada (HbA1c) confiere una importante reducción del riesgo de efectos adversos mayores, mientras que tal asociación no se ha observado en ensayos con el tratamiento tradicional (efectos secundarios entre los cuales se incluye la hipoglucemia).
| Hipoglucemia y enfermedad cardiovascular en poblaciones especificas |
Muchas guías de práctica clínica recomiendan evitar el control glucémico estricto en personas mayores (por ej., >75 años) con diabetes, y personas frágiles con comorbilidades y enfermedad crónica terminal. En estas poblaciones, el control estricto no ha mostrado beneficios, al mismo tiempo que se ha observado un aumento potencial del daño, en gran parte relacionado con la hipoglucemia.
A pesar de estas recomendaciones, es común que estos pacientes reciban un tratamiento excesivo, particularmente con insulina o sulfonilureas. Como era de esperar, este tratamiento excesivo aumenta el riesgo de hipoglucemia asociada al aumento de la edad en sí, una carga elevada de comorbilidades, disminución de la capacidad cognitiva y disminución e la función renal. Paradójicamente, en esta población, el control glucémico más flexible también se asocia con hipoglucemias.
En estudios de observación se ha identificado una asociación entre la hipoglucemia y la mortalidad en ancianos, pero no se ha evaluado adecuadamente su asociación con la enfermedad cardiovascular, requiriéndose más estudios en poblaciones <75 años.
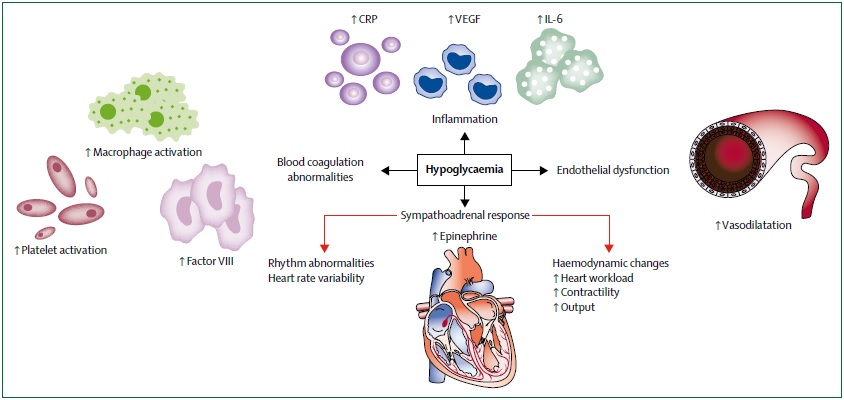
Consecuencias cardiovasculares fisiopatológicas de la hipoglucemia.
| Embarazo |
La incidencia global de infarto agudo de miocardio aumenta de 3-5 veces durante el embarazo, particularmente en mujeres con diabetes preexistente; el riesgo de mortalidad es elevado en pacientes con diabetes e infarto de miocardio.Los autores no han hallado reportes de interacción entre la hipoglucemia y la cardiopatía isquémica durante el embarazo, pero la hipoglucemia grave es muy frecuente en las mujeres embarazadas con diabetes tratadas con insulina, particularmente en el primer trimestre.
La asociación no puede ser usada como un argumento en contra del manejo intensivo de la glucemia durante el embarazo, ya que sus beneficios para el feto son muy claros, pero requiere mayor atención para alcanzar la normoglucemia sin sufrir hipoglucemia en exceso.
> Niños y adolescentes
Hay pocos datos sobre las consecuencias cardiovasculares de la hipoglucemia en niños y adolescentes con diabetes. Aunque es especulativo, el efecto más probable de la hipoglucemia en el sistema cardiovascular en menores de 18 años es la muerte súbita inesperada en la cama (síndrome de muerte en la cama).
En niños y adolescentes, los datos de mortalidad son limitados, pero la mortalidad en esta población comparada con la población general de la misma edad es significativamente más elevada.
Es menos probable que haya un sub-informe de muerte relacionada con diabetes de niños y adolescentes debido a las tasas más bajas de comorbilidad comparados con los adultos. La mayoría de los informes describen un aumento de 2-4 veces la mortalidad estandarizada en niños y adolescentes con diabetes tipo 1.
La cetoacidosis diabética es la causa de muerte más frecuente, pero la hipoglucemia y el síndrome de muerte en la cama también figuran en la mayoría de las encuestas. La muerte asociada con hipoglucemia en niños y adolescentes puede estar seguida de una convulsión, o provocar un accidente o ahogamiento y podría no invocar una causa cardiovascular.
| Efectos cardiovasculares de la hipoglucemia |
La hipoglucemia activa el sistema simpático suprarrenal causando una profusa secreción de catecolaminas que ejercen importantes efectos hemodinámicos y hemorreológicos. La estimulación simpática provoca un rápido incremento de la frecuencia cardíaca, contractilidad miocárdica y gasto cardíaco, y la presión sistólica central cae debido al aumento de la elasticidad de los grandes vasos.
El potasio plasmático desciende rápidamente, induciendo cambios electrofisiológicos y electrocardiográficos que podrían provocar conducción y repolarización cardíacas anormales.
Por otra parte, en respuesta a la hipoglucemia se producen cambios agudos en lacoagulabilidad de la sangre, adhesión celular, disfunción endotelial e inflamatoria y marcadores. Estos efectos tienen el potencial de comprometer la función endotelial, el flujo sanguíneo y la perfusión tisular, con riesgo de coagulación intravascular y trombosis.
El antecedente de hipoglucemia atenúa la respuestas autonómica al estrés cardíaco durante varias horas en personas sin diabetes, y este deterioro transitorio de los reflejos cardíacos autonómicos podría afectar la vulnerabilidad cardíaca a un estrés posterior.
En pacientes con diabetes tipo 2, la hemorreología y las respuestas inflamatorias a la hipoglucemia persisten durante varios días.Las anomalías funcionales que persisten mucho tiempo después de la restauración de la normoglucemia podrían crear un medio intravascular propicio para un evento trombótico.
Paradójicamente, en el ensayo ACCORD, la hipoglucemia grave que se asoció a mortalidad cardiovascular fue observada en pacientes bajo tratamiento estándar que mantuvieron concentraciones de HbA1c más elevadas que en los tratados intensivamente.
No está claro si la exposición frecuente a la hipoglucemia aumenta el riesgo de eventos cardiovasculares o si, incluso, podría tener un efecto protector a través de una menor respuesta simpático suprarrenal por hipoglucemia repetida.
En diabéticos tipo 2, muchos de los cuales tienen enfermedad cardiovascular prematura, los cambios hemodinámicos transitorios asociados con hipoglucemia pueden provocar eventos cardiovasculares agudos como infarto de miocardio, insuficiencia cardíaca y arritmias cardiacas.
Se han descrito algunos casos de eventos cardiovasculares agudos precipitados por la hipoglucemia; también se han informado cambios electrocardiográficos isquémicos, con y sin el desarrollo de angina.
| Mecanismos potenciales |
La hipoglucemia es un estrés sistémico profundo, que tiene efectos substancialmente hemodinámicos, proinflamatorios y pro-aterotrombóticos, así como el aumento del potencial de arritmias cardíacas.
La hipoglucemia también estimula el aumento de aldosterona plasmática mediante la activación del sistema renina-angiotensina, el cual, activando al receptor mineralocorticoide, podría exacerbar la disfunción endotelial.
La mayor carga de trabajo cardíaco durante la hipoglucemia aguda se acompaña de cambios en la hemorreología vascular, con aumento de la activación plaquetaria, disminución del equilibrio fibrinolítico y elevación de la hemostasia.
Sin embargo, la hipoglucemia recurrente inhibe la respuesta simpático suprarrenal a la hipoglucemia y disminuye la sensibilidad β-adrenérgica. Así, los efectos hemodinámicos de la hipoglucemia podrían ser paradójicamente menos profundos en las personas con mayor riesgo de hipoglucemia grave.
La hipoglucemia aguda también provoca una respuesta proinflamatoria que podría contribuir a la disfunción endotelial y ser pro-aterogénica.
En individuos con y sin diabetes, la hipoglucemia provoca mayor expresión del clúster de diferenciación 40 (CD40) en los monocitos y concentraciones del ligando CD40 solubles plasmático, así como el aumento de la molécula de adhesión intercelular 1, proteína de adhesión a células vasculares 1, selectina E, factor de crecimiento del endotelio vascular y, las citocinas interleucina-6 y -8 y, factor de necrosis tumoral α.
Esta respuesta proinflamatoria podría empeorar la inflamación crónica y la disfunción endotelial, común en la diabetes. Ciertamente, la disfunción endotelial con alteración de la vasodilatación mediada por el óxido nítrico es evidente durante la hipoglucemia y se exacerba después de 2 episodios de hipoglucemia.
La hipoglucemia repetida en la diabetes tipo 1 también se asocia con disfunción endotelial mediada por flujo y aumento del espesor de la íntima-media. Sin embargo, esta respuesta puede ser modificada por la exposición recurrente a la hipoglucemia.
Ratter y col. han demostrado que en personas sin diabetes y personas con diabetes tipo 1, la hipoglucemia promovió la movilización de subgrupos específicos de leucocitos e indujo cambios proinflamatorios en las células inmunes con respuestas exageradas de las citocinas a la estimulación microbiana.
Sin embargo, aunque la hipoglucemia puede activar múltiples vías que potencialmente conducen a la disfunción endotelial, una respuesta similar a la hipoglucemia aguda en términos de citocinas inflamatorias y liberación de selectina se ve durante el ejercicio agudo en personas sin diabetes, con y sin enfermedad coronaria y generalmente, el ejercicio es considerado cardioprotector.
| Es importante reconocer que, tanto en la diabetes tipo 1 como tipo 2, la hipoglucemia ocurre en situaciones de exposición crónica a glucemias elevadas, y el tratamiento (o tratamiento excesivo) de la hipoglucemia suele provocar hiperglucemias de rebote. |
La diabetes preexistente también empeora los resultados cardíacos en un modelo de roedores de exposición a hipoglucemias muy severas. Estas observaciones sugieren que la capacidad de las defensas del huésped para hacer frente al estrés hipoglucémico se ve afectada por la diabetes preexistente y que la respuesta inflamatoria a la hipoglucemia podría ser amplificada por la hiperglucemia de rebote en el período de recuperación.
Se han reportado episodios clínicos de hipoglucemia que causan fibrilación auricular, latidos ectópicos ventriculares múltiples y taquicardia ventricular.Un informe fundamental de Tattersall y Gill de 1991 brindó importante evidencia de que la hipoglucemia estuvo implicada en la muerte súbita de la noche a la mañana de jóvenes con diabetes tipo 1. Este modo de muerte, descrito como síndrome de muerte en la cama, ha sido reportado en una serie de estudios epidemiológicos.
Se considera que la arritmia es una causa de muerte probable. Un ejemplo de muerte súbita durante una hipoglucemia grave es el caso de un joven de 23 años con diabetes tipo 1, cuyo monitoreo continuo de la glucosa demostró hipoglucemia en el momento de la muerte. Se destaca que en la autopsia de este individuo por lo demás sano no se halló ninguna causa de muerte posible, arribándose al diagnóstico de muerte por arritmia cardíaca.
Se ha demostrado que la hipoglucemia Inducida experimentalmente en personas con diabetes tipo 1 y tipo 2 provoca una repolarización cardíaca pro-arritmogénica, con prolongación del Intervalo QT corregido para la frecuencia cardíaca. Se ha postulado que las personas con polimorfismos de los canales iónicos, los cuales contribuyen al desarrollo del sistema de conducción cardíaca, podrían ser particularmente vulnerables.
Otros estudios experimentales y de observación han demostrado anomalías de la repolarización cardíaca junto con marcada bradicardia en algunos individuos susceptibles con diabetes tipo 1, pero se desconoce qué es lo que confiere susceptibilidad o desencadena el evento fatal.
La hipoglucemia grave (<18 mg/dl) en modelos de roedores se asoció con prolongación del intervalo QT, ectopia ventricular y bloqueo cardíaco de alto grado, dependiente de la duración y gravedad de la hipoglucemia. Curiosamente, la mortalidad en este modelo de hipoglucemia grave en roedores fue exacerbada por la diabetes, pero en su mayor parte revertida por la exposición previa a hipoglucemias recurrentes y reemplazo de potasio; la infusión de glucosa en los ventrículos cerebrales o el bloqueo adrenérgico β redujo las arritmias inducidas por hipoglucemia grave y, la mortalidad global.
Las arritmias inducidas por hipoglucemia grave también son un potencial contribuyente al aumento de la mortalidad cardíaca observada en el estudio ACCORD. Estudios en pacientes ambulatorios combinando el monitoreo Holter y la medición de la glucosa intersticial continua han documentado un aumento relativo de la frecuencia de la bradicardia y la actividad ectópica auricular durante la hipoglucemia.
En un estudio detallado de los efectos arrítmicos de la hipoglucemia en personas con diabetes tipo 2 realizado con una pinza hipoglucemiante, Chow y col. demostraron que la inhibición vagal inicial durante la hipoglucemia dio lugar a un aumento de la frecuencia cardíaca, pero con una hipoglucemia más prolongada, la posterior reactivación vagal dio lugar a una bradicardia relativa, consistente con las observaciones anteriores. Por el contrario, las personas sin diabetes del estudio tuvieron una taquicardia persistente durante la hipoglucemia, lo que implica una inhibición vagal continua.
Estos autores también señalaron que las personas con diabetes tipo 2 tuvieron mayor frecuencia cardíaca, menor variabilidad de la frecuencia cardíaca, y mayores cambios en la duración y heterogeneidad de las anomalías de la repolarización durante la hipoglucemia.
Por qué las personas con diabetes tipo 2 responden de manera diferente a la hipoglucemia en este contexto no se sabe, pero se ha demostrado que la hipoglucemia reduce la sensibilidad del barorreflejo, aumenta el umbral de presión arterial para la activación del barorreflejo, y reduce el rango de respuestas del intervalo R-R. Así, las anomalías preexistentes de la función autonómica podrían contribuir a una mayor propensión a las arritmias cardíacas.
| Enfoques clínicos |
Las consecuencias negativas de la hipoglucemia, que van desde síntomas desagradables a situaciones potencialmente peligrosas, suelen hacer que los pacientes y sus familiares desarrollen miedo a la hipoglucemia.
Numerosos estudios han documentado el efecto perjudicial del miedo a la hipoglucemia sobre la calidad de vida en diferentes países y culturas. En general, los niveles de miedo a la hipoglucemia elevados se asocian más comúnmente a una historia de episodios de hipoglucemia grave, especialmente los que provocan:
- desorientación cognitiva
- vergüenza social
- pérdida de la conciencia
- accidentes y lesiones físicas
Los padres de niños con diabetes tipo 1 son particularmente vulnerables a los altos niveles de temor a la de hipoglucemia, incluyendo la ansiedad relacionada con los episodios nocturnos de hipoglucemia.
El miedo a la hipoglucemia también podría tener consecuencias en el manejo y control de la diabetes. Algunos pacientes pueden hacer frente a su miedo y tratar de mitigar la amenaza de hipoglucemia manteniendo su glucemia en un rango más elevado, lo que lleva a una pérdida de tiempo adicional por la hiperglucemia.
Varios estudios han demostrado que los niveles elevados de miedo a la hipoglucemia se asocian con un control metabólico más deficiente, incluyendo lecturas más frecuentes de la glucemia y niveles más elevados de la HbA1c.
Aunque los pacientes pueden ser reacios a informar los episodios de hipoglucemia grave a sus médicos, es crucial evaluar estos episodios en entornos clínicos. Además de evaluar factores tales como etiología, frecuencia y gravedad, es importante interrogar a los pacientes y familiares sobre aspectos del episodio.
Es probable que se asocien con efectos psicológicos, dependiendo sobre todo de la situación en que se presentan (lugar público o si está solo), las implicancias sociales (por ej., frente a amigos o colegas), y consecuencias emocionales (nivel de temor o peligro percibido) del episodio. Los cambios que han hecho los pacientes o familiares en el manejo de la diabetes y la rutina en respuesta a un episodio de hipoglucemia también deben ser cuidadosamente evaluados.
El raro, pero reconocido, síndrome de la muerte en la cama presenta un problema especial y un dilema ético para los profesionales de la salud, en relación con la educación sobre la hipoglucemia del paciente y la familia. Los autores no hallaron estudios que hayan explorado específicamente el efecto potencial de la mortalidad secundaria a la hipoglucemia en la familia de los afectados.
Sin embargo, muchos pacientes y sus familias están preocupadas por la posible ocurrencia de una hipoglucemia grave nocturna fatal, especialmente si han presenciado una convulsión hipoglucémica.
Aunque no hubo investigación aparente sobre los efectos psicológicos en las familias de los pacientes, hay evidencia anecdótica de que en las conversaciones con pacientes y familiares, la mayoría de los médicos no plantea el tema de las arritmias cardíacas fatales causadas por la hipoglucemia.
Aunque la hipoglucemia nocturna es frecuente, los episodios fatales son muy raros. Así, presentándolo como un resultado posible podría producir elevados niveles de ansiedad injustificados.
Se requieren investigaciones adicionales para comprender los factores de riesgo y los mecanismos asociados a la hipoglucemia nocturna fatal, lo que ayudaría a orientar el desarrollo de la educación y las recomendaciones adecuadas para el paciente.
| Enfoques clínicos básicos |
Los médicos que prescriben insulina y sulfonilureas deben preparar a los pacientes para la hipoglucemia, la cual podría ocurrir al utilizar estos medicamentos.Cuando la carga laboral del consultorio es grande, estos pacientes deben ser derivados para recibir educación diabetológica y una instrucción integral para el reconocimiento, anticipación y tratamiento de la hipoglucemia. Una habilidad clínica necesaria para todos los médicos es aprender a identificar a las personas con poca capacidad para reconocer la hipoglucemia.
Podrían considerar el uso de cuestionarios desarrollados por el grupo de trabajo ADA Hypoglycaemia Working Group para garantizar la realización de una evaluación sistemática en cada visita. El International Hypoglycaemia Study Group también ha desarrollado materiales educativos para médicos y pacientes, con el fin de mejorar la comprensión de esta complicación del tratamiento de la diabetes. Los avances en el cuidado de la diabetes han proporcionado nuevos enfoques que reducen el riesgo de hipoglucemia en pacientes con diabetes.
Los pacientes con diabetes tipo 1 y tipo 2 que requieren insulina podrían hallar que tienen menos hipoglucemia si usan una insulina basal de acción prolongada, como la insulina degludec, que reduce las tasas de hipoglucemia en ambos tipos de diabetes, en comparación con la insulina glargina U100.
Los individuos con diabetes tipo 1 que tienen mayor riesgo de hipoglucemia podrían beneficiarse con una bomba de insulina y el agregado del monitoreo continuo de la glucosa (MCG) en tiempo real al régimen de insulina existente, ya que también se ha demostrado que disminuye la hipoglucemia.
El uso de una bomba con umbral de suspensión o una bomba híbrida de circuito cerrado puede reducir las tasas de hipoglucemia en pacientes con diabetes tipo 1, sin poner en peligro el control glucémico.
Los pacientes con poca conciencia de hipoglucemia y episodios repetidos de hipoglucemia grave, a pesar de los esfuerzos para evitarla, podrían ser elegibles para el trasplante de islotes, cuando esté disponible.
| Reducción de la hipoglucemia en pacientes con riesgo cardiovascular elevado |
Los estándares de atención de la ADA recomiendan cambiar los objetivos glucémicos en pacientes que tienen hipoglucemia clínicamente significativa o alteración de la conciencia de hipoglucemia.Para los pacientes que reciben insulina o sulfonilureas debe haber un mayor énfasis en las comorbilidades cardiovasculares y, si es necesario, desplazar los objetivos glucémicos hacia arriba y los objetivos de la HbA1c a un 7,5% para ayudar a los pacientes vulnerables a que no sufran hipoglucemias.
En pacientes con diabetes tipo 2, la reducción del riesgo de hipoglucemia podría lograrse cambiando a un régimen que no incluya insulina o sulfonilureas, lo que también permitiría los beneficios de alcanzar una HbA1c más baja.
Aunque el uso de nuevas tecnologías incluye las bombas, el MCG y análogos de la insulina podría reducir la incidencia de hipoglucemia, no hay evidencia de que esto se traduzca en menor riesgo de enfermedad cardiovascular o que mejore la supervivencia en personas con diabetes, tal vez debido a la corta duración de los ensayos y el bajo riesgo cardiovascular basal de los participantes del estudio.
Los estudios que se ha acercado más a encontrar tal efecto fueron el ensayo DEVOTE (ensayo comparativo de seguridad cardiovascular de la insulina degludec vs. la insulina glargina en sujetos con diabetes tipo 2 y riesgo elevado de eventos cardiovasculares).
En el ensayo, realizado en pacientes con diabetes tipo 2 y mayor riesgo de enfermedad cardiovascular, la insulina degludec (comparada con la insulina glargina U100) redujo la incidencia de hipoglucemia grave en un 40%, así como un 9% no significativo redujo la incidencia de eventos de enfermedades cardiovasculares.
| Direcciones futuras |
Es posible que las respuestas a la hipoglucemia no grave documentadas puedan ser exageradas y algunos efectos solo puedan ocurrir durante la hipoglucemia agrave. Por otra parte, no se conoce la duración de las posibles respuestas adversas .
Este tema es importante ya que es menos probable que la respuesta inflamatoria procoagulante muy transitoria aumente el riesgo de morbilidad cardiovascular que uno más prolongado. Tampoco está claro si la exposición repetida a hipoglucemias moderadas tiene un efecto acumulativo. Se necesita comprender mejor los factores de modulación para explicar la relación entre la hipoglucemia y el riesgo de enfermedad cardiovascular.
En el estudio ADVANCE, solo los niveles plasmáticos de IL-6, pero no los de la proteína C reactiva o del fibrinógeno, se asociaron de forma independiente con eventos o muerte en pacientes con diabetes tipo 2.
En el estudio de diabetes tipo 2 de Edimburgo no hubo evidencia de un aumento de los niveles de factores inflamatorios que afecten la relación entre la hipoglucemia grave y las complicaciones cardiovasculares en diabéticos tipo 2. Tampoco está claro cuánto tiempo persisten las condiciones proinflamatorias y la menor función endotelial después de la resolución de la hipoglucemia.
Se ha sugerido que las modificaciones del epigenoma inducidas por la hiperglucemia son las responsables del fenómeno de la memoria glucémica, es decir, la observación que el daño vascular causado por la hiperglucemia crónica anterior persiste a pesar del buen control glucémico actual. Los factores epigenéticos también podrían contribuir a los efectos de la hipoglucemia en el sistema cardiovascular.
Se necesitan las técnicas de imagen de vanguardia (PET, resonancia magnética funcional, espectroscopia de resonancia magnética) para visualizar con mayor precisión cómo la hipoglucemia afecta la perfusión cardíaca y cerebral y la captación y metabolismo de los nutrientes en estos órganos.
También es importante establecer si los efectos de los episodios recurrentes de hipoglucemia son acumulativos o diminutivos.
Se ha demostrado que en personas sanas, la exposición a dos episodios consecutivos de hipoglucemia no ocasionan mayor deterioro de la función endotelial que un solo episodio, aunque este no fue el caso para la elevación de las citocinas proinflamatorias.
Por el contrario, se ha informado que las respuestas inflamatorias agudas a la hipoglucemia fueron más atenuadas en los pacientes con diabetes tipo 1 y deterioro de la conciencia de la hipoglucemia, posiblemente debido a la reducción de la respuesta hormonal contrarreguladora.
En las ratas, la hipoglucemia recurrente protege contra la muerte inducida por hipoglucemia o los daños neuronales, en lugar de amplificar el riesgo de estos eventos. A la inversa, una respuesta hormonal contrarreguladora exagerada, particularmente de epinefrina y cortisol, podría explicar porqué los pacientes con control glucémico deficiente podrían estar en mayor riesgo cuando se exponen a un episodio hipoglucémico.
La investigación experimental en hipoglucemia grave se ha hecho principalmente en modelos de rata. Tales experimentos no pueden emprenderse en seres humanos por razones éticas, y la replicación debe buscarse en modelos animales más grandes, con la función cardiovascular que mejor se asemeje a la fisiología humana.
Poco se sabe acerca de las diferencias en la vulnerabilidad a los efectos cardiovasculares potencialmente perjudiciales de la hipoglucemia iatrogénica, o de los mecanismos subyacentes, entre los subgrupos de pacientes. Por ejemplo, es poco probable que la hipoglucemia ejerza el mismo efecto, o la misma respuesta cardiovascular, en los jóvenes con diabetes tipo 1 por lo demás sanos, que en las personas mayores con diabetes tipo 2 y aterosclerosis avanzada.
La susceptibilidad a las arritmias cardíacas durante las hipoglucemias parece estar confinada a unos pocos individuos, y se desconoce la causa de la susceptibilidad y cómo proceder para identificar a los pacientes que están en mayor riesgo.
La identificación de las personas con mayor riesgo de arritmias durante la hipoglucemia es obviamente importante, con respecto al equilibrio de los beneficios de la optimización del control glucémico contra los riesgos de la hipoglucemia.
Por otra parte, comprobar que estos efectos están presentes en individuos sin comorbilidades ayudaría a establecer que la hipoglucemia es un factor de riesgo y no simplemente un marcador de riesgo.
*Resumen objetivo y traducción Dra. Marta Papponetti
Contenidos relacionados
Los editores le recomiendan continuar con las siguientes lecturas:






















.png)










No hay comentarios:
Publicar un comentario