
Consenso de expertos de la European Society of Cardiology | 21 JUL 19
Cuarta definición universal del infarto agudo de miocardio
Incorpora la nueva clasificación del IAM, así como su diagnóstico en diversas situaciones clínicas con utilidad práctica
Autor: hygesen K, Alpert JS, Jaffe AS, Chaitman BR, Bax JJ, Morrow DA y col. European Heart Journal 2019; 40:237-269.
Texto principal
| Introducción |
Aquí se presenta el Fourth Universal Definition of Myocardial Infarction Consensus Document, que incorpora la nueva clasificación del IAM, así como diversas situaciones clínicas de daño y IAM.
| Características anatomopatológicas de la isquemia y del IAM |
La microscopía electrónica muestra alteraciones de la mitocondria. La necrosis de los miocitos se produce después de varias horas y progresa desde el subendocardio hacia la superficie. La implementación en tiempo adecuado de las técnicas de reperfusión, reduce el daño.
| Biomarcadores de daño y de IAM |
Los biomarcadores preferidos para evaluar el daño miocárdico son cTn y cTnT. También se recomienda la cTn de alta sensibilidad (hs-cTn). La CK-MB es menos sensitiva y menos específica.
El criterio de daño miocárdico se establece cuando los valores de cTn se encuentran por encima del percentilo 99 del límite superior de referencia.
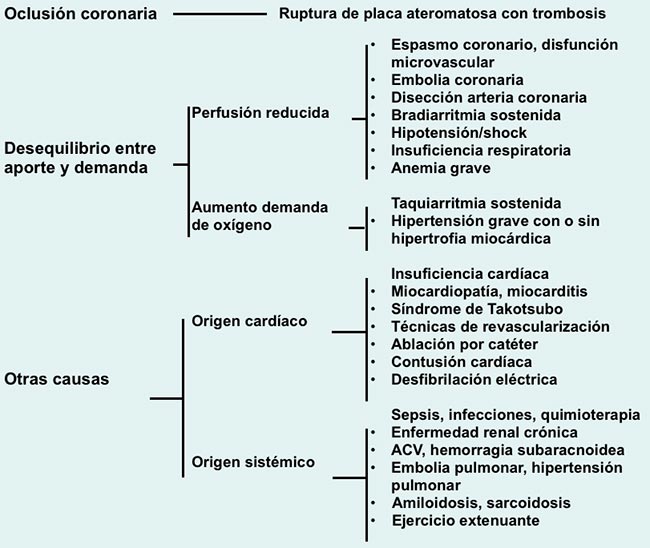
El daño puede ser agudo cuando se detecta un nuevo ascenso dinámico y/o caída de los valores de cTn, o crónico ante la persistencia de valores de cTn aumentados por encima del percentilo 99. Los mecanismos que pueden producir daño miocárdico con aumento de cTn son (Figura 1):
| Cuadro clínico del IAM |
- La isquemia miocárdica se identifica por los antecedentes y el electrocardiograma (ECG).
- Los síntomas de dolor pueden estar referidos a la región precordial, la extremidad superior, la mandíbula, malestar epigástrico durante el ejercicio o en reposo o los equivalentes isquémicos de fatiga y disnea.
- La tríada clásica es el dolor, el ECG patológico y el aumento o la caída de cTn.
| Clasificación clínica del IAM |
IAM tipo 1. Causado por la ruptura de una placa inestable y trombosis coronaria.
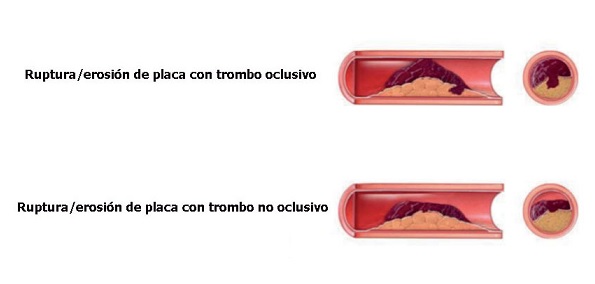
Figura 2. IAM tipo 1. Elaborado sobre el contenido del artículo del European Heart Journal 2019;40:237-269.

Figura 3. Criterios para IAM tipo 1. La presencia de oclusión coronaria por trombo o una zona extensa de necrosis está dentro de los criterios de IAM tipo 1, independientemente de la cTn.
IAM tipo 2. Es producido por un desequilibrio entre la oferta y la demanda de oxígeno (ver Figura 1 sobre las distintas causas). Este tipo de IAM es más frecuente en las mujeres y tiene tendencia a mayor mortalidad que el tipo 1 debido a las morbilidades asociadas que son los factores causales (Figura 4).
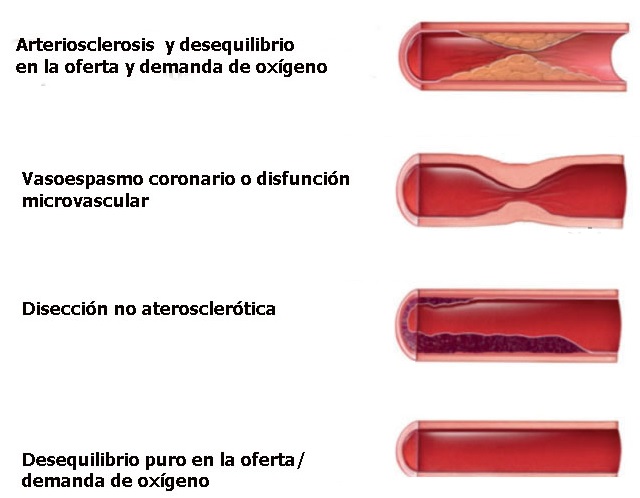

En este tipo de IAM es importante tratar la causa subyacente que produce el desequilibrio entre la oferta y la demanda de oxígeno (aporte de plasma, sangre, control de la arritmia y apoyo respiratorio).
IAM tipo 3. Se trata de pacientes que presentan síntomas de IAM, cambios del ECG o fibrilación ventricular y fallecen antes de que se produzcan alteraciones de cTn. En estos casos la autopsia puede mostrar una obstrucción coronaria total por accidente de placa o trombo y se lo reclasifica como IAM tipo 1.
IAM post procedimiento de revascularización. La Figura 6 muestra los criterios


IAM asociado con angioplastia intraluminal coronaria (AIC) IAM tipo 4

Figura 7. Criterios de IAM tipo 4. La presencia aislada de ondas Q patológicas participa del criterio de IAM tipo 4 si los valores de cTn están aumentados, pero menos de 5 veces el percentilo 99. También se incluyen dentro del IAM tipo 4 las demostraciones post-mortem de trombo en la arteria tratada o un área extensa de necrosis con hemorragia intramiocárdica o sin ella.
| IAM asociado con trombosis del stent. IAM tipo 4b |
- aguda (0-24 horas);
- subaguda > 24 horas a 30 días;
- tardía > 30 días a 1 año;
- muy tardía (> 1 año).
| IAM asociado con cirugía de revascularización coronaria. IAM tipo 5 |

Figura 8. Criterios de IAM tipo 5.
| Reinfarto |
El reinfarto se debe considerar cuando reaparece un supradesnivel ST ≥ 1 mm o nuevas ondas Q patognomónicas en al menos 2 derivaciones sucesivas, especialrmente cuando se asocia con síntomas isquémicos. Un nuevo aumento del segmento ST también se puede ver en amenaza de ruptura miocárdica o en la pericarditis.
Se recomienda una determinación inmediata de cTn y repetir 3 a 6 horas después. Si en la muestra inicial existe aumento de cTn, pero se encuentra estable o en disminución, en la segunda muestra debe haber aumento > 20% de cTn.
| Daño miocárdico e IAM asociado con otros procedimientos cardíacos |
El tratamiento de arritmias por ablación produce daño miocárdico controlado por la aplicación de calor o frío en el tejido. La extensión del daño se determina por el aumento de cTn, pero se considerará IAM si se cumplen los criterios del biomarcador correspondientes al tipo 5 de IAM.
| Daño miocárdico e IAM asociado con procedimientos quirúrgicos extracardíacos |
El conocimiento de los valores basales de hs-cTn puede ayudar a identificar a los pacientes con aumento crónico de cTn antes de la cirugía y durante y después de la operación.
La determinación de hs-cTn en las muestras postoperatorias revelan que el 35% de los pacientes tiene valores superiores al percentilo 99 y alrededor del 17% muestran un patrón de ascenso que sugiere un IAM en evolución. Estos últimos son los pacientes de alto riesgo de IAM.
El diagnóstico se complementa con el ECG. En el paciente de alto riesgo que será sometido a cirugía mayor, se recomienda determinación previa de c-TN y pesquisa postoperatoria del biomarcador.
| Lesión miocárdica o IAM en la insuficiencia cardíaca |
| Síndrome de Takotsubo |
Pasadas las 12-24 horas, se observan ondas T invertidas profundas y simétricas y prolongaciones del QTc. La determinación de cTn es de valor relativo, o sea que existe una distorsión en la relación entre los hallazgos del ECG y la bioquímica.
La coronariografía suele ser normal o la posible suboclusión no explica la extensa alteración en la motilidad del ventrículo. La función ventricular queda alterada durante varios días.Este síndrome se observa en el 1-2% de los pacientes con IAMSST y se suele desencadenar por estrés físico o emocional intenso.
En más del 90% de los casos se observa en mujeres postmenopáusicas y la mortalidad es semejante al IAMSST y es causada por shock cardiogénico, ruptura ventricular o arritmias malignas.
| IAM sin obstrucción coronaria |
La prevalencia es del 6-8% entre los pacientes con IAM, es más frecuente en las mujeres y en pacientes con NSST.
Las causas pueden ser ruptura de placa vulnerable seguida de trombosis, espasmo coronario y disección coronaria.
| IAM asociado con enfermedad renal crónica |
| Injuria e IAM en pacientes graves |
Estos pacientes pueden evolucionar hacia un IAM tipo 2 por desequilibrio en la demanda de oxígeno o también IAM tipo 1 por ruptura de placa vulnerable. Otros pacientes pueden tener aumento de cTn con baja fracción de eyección debido a sepsis causada por endotoxinas con recuperación del cuadro hemodinámico después del tratamiento exitoso de la sepsis.
| Enfoque bioquímico en el diagnóstico de injuria y de IAM |
Por ejemplo, alrededor de los valores pico .puede ser difícil observar un patrón cambiante de valores. Asimismo, la curva de descenso de concentración en el tiempo es mucho más lenta que la de ascenso. Estos aspectos se deben tener en consideración al definir si existe un patrón cambiante.
La sensibilidad analítica (límite de detección) de cTn y de cTnT tiene una variación de 10 puntos. Debido a que las determinaciones no están estandarizadas, los valores entre distintas determinaciones no pueden ser directamente comparables con los de otros trabajos.
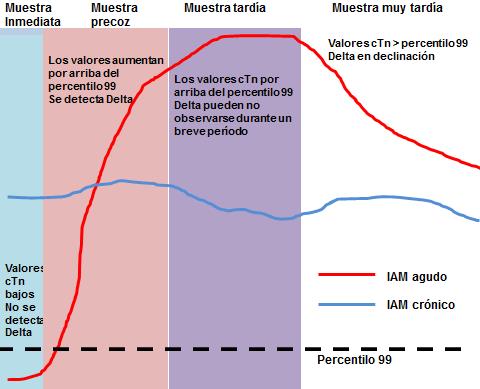
Figura 9. Curva cinética de la troponina cardíaca (cTn) después de producido un IAM. El tiempo de liberación del biomarcador en la circulación depende del flujo sanguíneo y la precocidad de la extracción una vez que se presentaron los síntomas. Los cambios (deltas) en los valores de cTn sirven para comparar entre episodios agudos y crónicos.
| El ECG en el IAM |
En los pacientes con síntomas persistentes o recurrentes o con un ECG inicial dudoso, se recomiendan determinaciones de ECG con intervalos de 15-30 minutos durante las dos primeras horas para detectar cambios dinámicos en los trazados.
Cambios importantes del segmento ST o inversiones de la onda T en numerosas derivaciones, se asocian con mayor grado de isquemia y peor pronóstico. Por ejemplo, un infradesnivel ST ≥ 1 mm en seis derivaciones, con probable asociación de supradesnivel ST en aVR o D1 asociado con compromiso hemodinámico sugiere lesión de varias coronarias o lesión de tronco de la coronaria izquierda.
Las ondas Q patológicas aumentan el riesgo quirúrgico.Otros signos asociados con isquemia aguda son: arritmias, bloqueos de rama, retardo de la conducción auriculoventricular y pérdida de la amplitud de R.
Las alteraciones del ECG no son patognomónicas de isquemia o IAM, ya que pueden observarse en pericarditis, hipertrofia ventricular izquierda, bloqueo de rama izquierda, síndrome de Brugada y síndrome de Takotsubo.
Un supradesnivel ST convexo prolongado, particularmente asociado con depresión recíproca del ST, señala oclusión coronaria con evolución hacia el daño y el IAM. Los cambios recíprocos permiten diferenciar IAMSST de la pericarditis o cambios precoces de repolarización. Las ondas Q también se presentan durante la fibrosis miocárdica en ausencia de enfermedad coronaria.
Un aumento hiperagudo de la amplitud de la onda T con ondas T simétricas prominentes en al menos 2 derivaciones, es un signo precoz que antecede al supradesnivel del segmento ST. En general, la aparición de nuevas onda Q indican necrosis miocárdica que se inician minutos/horas después del daño.
El punto J (la unión entre la terminación del QRS y el inicio del ST), determina la magnitud de los cambios del ST con el inicio del QRS como punto de referencia.
En los pacientes con línea de base estable, el segmento TP (intervalo isoeléctrico) es un método bastante preciso para determinar la magnitud de las desviaciones del ST y permite distinguir la pericarditis (depresión de PT) de la isquemia miocárdica aguda.
Una oclusión importante de la arteria coronaria descendente anterior se caracteriza por:
- En derivaciones precordiales: ausencia de supradesnivel ST, ondas T altas y simétricas, infra desnivel ST > 1 mm en el punto J.
- En aVR: supra desnivel ST > 1 mm.
- En derivaciones precordiales anteriores: inversiones simétricas (> 2 mm) de la onda T.
Diagnóstico de infarto de miocardio silente:
- Ondas Q en DV2, D3 > 0,02 s o complejo QS em D2, D3.
- Ondas Q ≥ 0,03 s y ≥ 1 mm de profundidad o complejos QS en D1, D2, AVL, AVF o V4-V6.
- Estudios por imágenes: adelgazamiento regional del ventrículo izquierdo, cicatriz o reducción de la motilidad de la pared por ecocardiograma, gammagrafía de perfusión miocárdica, tomografía computarizada de emisión de fotón único (SPECT [por las siglas en inglés]), tomografía de emisión de positrones (PET [por las siglas en inglés]) o resonancia magnética.
| Técnicas por imágenes |

Figura 10. Técnicas por imagen





















.png)










No hay comentarios:
Publicar un comentario