
Tras el coronavirus, nuevas ideas para los estudios clínicos del cáncer
, por el Equipo del NCI
Cuando la pandemia del coronavirus llegó a los Estados Unidos, miles de personas participaban en los estudios clínicos, como muchos en el St. Jude Children's Research Hospital, un hospital de investigación infantil en Memphis (Tennessee).
Con el propósito de evitar la infección por el virus que causa la COVID-19, los investigadores de St. Jude tomaron medidas para disminuir el riesgo para los niños que participaban en los estudios clínicos, incluso los estudios en los que se probaban nuevos medicamentos contra el cáncer. Una de las estrategias para evitar infecciones fue limitar los viajes de los pacientes al hospital.
En vez de que los pacientes fueran al hospital para las evaluaciones de rutina, el personal de enfermería visitó a los pacientes que estaban con su familia en alojamiento provisto por St. Jude.
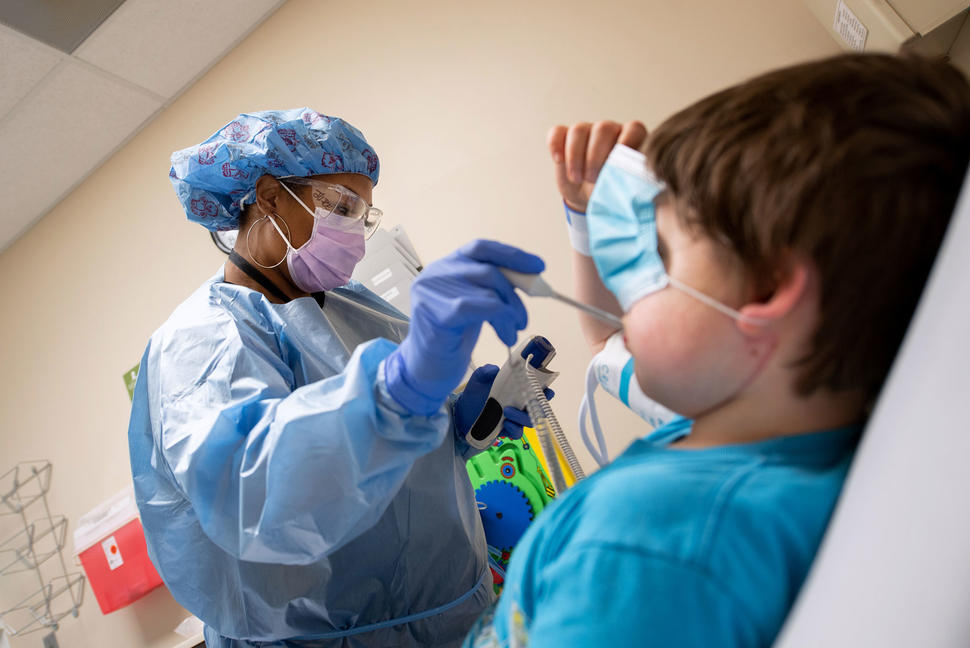
El personal de enfermería cargó sus mochilas con suministros médicos y equipo de protección personal y ofrecieron a los niños atención básica, como extracciones de sangre. En lo esencial, se llevaron los estudios clínicos a los pacientes. Durante la pandemia, esta idea genera mucho interés en los investigadores.
El personal de enfermería cargó sus mochilas con suministros médicos y equipo de protección personal y ofrecieron a los niños atención básica, como extracciones de sangre. En lo esencial, se llevaron los estudios clínicos a los pacientes. Durante la pandemia, esta idea genera mucho interés en los investigadores.
“Nos preocupa mucho que nuestros pacientes se expongan al nuevo coronavirus”, comentó la enfermera Robin Mutz, jefa ejecutiva de enfermería en St. Jude. Aunque St. Jude se mantuvo abierto durante la pandemia, los médicos prefirieron que los pacientes no fueran a las clínicas salvo que fuera indispensable, añadió.
Otro cambio que hizo St. Jude fue programar citas virtuales entre los proveedores de atención de la salud y los pacientes de los estudios de investigación, que también se llaman telesalud o telemedicina. En algunos casos, el personal tenía capacitación en telemedicina.
Para continuar con las consultas de telemedicina y las visitas virtuales de estudios de investigación después de la pandemia, destaca Mutz, hace falta que los cambios en la reglamentación sobre telemedicina durante la COVID-19 sean permanentes.
El aumento en el uso de la telemedicina es uno de los cambios favorables para los estudios clínicos que se podrían continuar después de que pase la pandemia, según los resultados de dos encuestas realizadas a investigadores de estudios clínicos y una serie de comentarios recientes de encargados de estudios clínicos.
Otros cambios en los estudios clínicos durante la pandemia que se podrían incorporar a los estudios son: las firmas electrónicas de los formularios de consentimiento de los pacientes, la supervisión a distancia de los resultados de los estudios clínicos y el envío de los medicamentos orales al domicilio de los pacientes que participan en los estudios clínicos.
“Aprendimos varias lecciones”, comentó el doctor William Dahut, director científico de investigación clínica en el Centro de Investigación Oncológica (CCR) del Instituto Nacional del Cáncer (NCI), quien lleva a cabo estudios clínicos. “Mi esperanza es que salgamos de esta etapa con mejoras en la forma que realizamos los estudios clínicos del cáncer”.
En el pasado, estos cambios se hubiesen considerado violaciones a los protocolos de los estudios. Pero en marzo, el NCI elaboró directrices para las actividades relacionadas con estudios clínicos afectadas por la pandemia del coronavirus. Por su parte, la Administración de Alimentos y Medicamentos (FDA) también publicó directrices sobre estudios clínicos de productos médicos durante la pandemia.
“Supervisamos con atención los estudios clínicos que patrocina el NCI a fin de entender cómo adaptarlos para que los pacientes sigan recibiendo atención mientras que los investigadores, en lo posible, continúan con los estudios clínicos”, explicó la doctora Meg Mooney, del Programa de Evaluación de Tratamientos del Cáncer (CTEP).
El NCI otorgó flexibilidad a los centros de estudios clínicos, incluso para los plazos en que se deben hacer las pruebas y evaluaciones de los pacientes.
“Los investigadores a cargo de los estudios clínicos pueden trabajar con el Consejo de Revisión Institucional (IRB) que supervisa el protocolo de cada estudio para hacer los ajustes necesarios”, explicó la doctora Mooney. “Estos cambios dan flexibilidad sin afectar la seguridad del paciente ni la validez de los datos que se recopilan mediante el estudio”.
“Lo desconocido”
Los estudios clínicos son esenciales para avanzar contra el cáncer. Estos estudios evalúan nuevas terapias y, con frecuencia, son la mejor opción o la única opción de tratamiento para algunos pacientes. Durante la pandemia, el NCI continuó con la inscripción de participantes en los estudios clínicos del Centro Clínico de los NIH en Bethesda (Maryland) cuando el Centro contaba con los tratamientos más adecuados.
La mayor dificultad que enfrentamos las primeras semanas de la pandemia fue "lo desconocido", comentó el doctor Dahut. Las restricciones de viaje y otras medidas para limitar la transmisión del nuevo coronavirus fueron un problema porque los pacientes viajaban desde lejos para ir a las consultas. ¿Debían estos pacientes viajar a Bethesda? ¿Debían recibir los tratamientos cada 6 semanas en vez de cada 4 semanas?
“Estábamos tratando de hallar el equilibrio entre ofrecer tratamiento de cáncer a los pacientes y mantener la seguridad de ellos al viajar", señaló. Además, los investigadores tampoco tenían mucha información para tomar estas decisiones.
Con la telemedicina, no hacen falta tantas consultas en persona en el Centro Clínico. Cuando los pacientes toman un medicamento nuevo, hay que verlos una vez por semana, dijo el doctor Dahut, pero casi siempre es posible hacer citas virtuales.
“Los investigadores con más experiencia tienen una buena idea de cómo está la persona al verla durante la consulta virtual”, explicó. Si hace falta, el paciente se podrá comunicar con un médico local para que lo atienda de inmediato.
Otra opción atractiva de la telemedicina es que los familiares que viven lejos del paciente pueden participar en las conversaciones con los médicos, destacó el doctor Dahut. También agregó que “con las tecnologías de la telemedicina, el médico puede invitar a los hijos a participar en la conversación enseguida. Esto permite que los hijos escuchen la charla y observen el lenguaje corporal del familiar".
A su vez, el doctor Dahut y sus colegas han tratado de limitar la cantidad obligatoria de pruebas y viajes que los pacientes deben hacer en el Centro Clínico sin que peligre la seguridad del paciente y sin que afecte la solidez de los estudios clínicos.
Para tal fin, los investigadores deben evaluar con atención a cada paciente y consultar con el Consejo de Revisión Institucional (IRB) y el patrocinador del estudio, según un comentario que escribió el doctor Dahut en colaboración con otros autores sobre la realización de estudios clínicos después de la pandemia de la COVID-19.
Encuestas que ofrecen un vistazo a los cambios en los estudios clínicos
Al comienzo de la pandemia, los dirigentes de la Sociedad Estadounidense de Oncología Clínica (ASCO) sabían que esta tendría repercusiones en los estudios clínicos y crearon una encuesta para registrar algunos de estos cambios. La encuesta se realizó a fines de marzo y obtuvo respuestas de 32 investigadores: 14 de programas académicos y 18 de programas comunitarios.
“Fue un vistazo a las observaciones y emociones de la gente en ese momento. Creo que sirve de motivación para lograr cambios que mejoren el sistema de investigación clínica”, comentó el doctor David Waterhouse, de Oncology Hematology Care en Cincinnati, uno de los encargados de la encuesta.
“Ante el desafío de ver y atender a los pacientes durante la pandemia, es probable que la telemedicina haya sido la solución de mayor uso”, continuó.
El doctor Waterhouse destaca que no todos los pacientes tienen la posibilidad de viajar a los centros oncológicos para recibir tratamiento y esto crea desigualdades en la atención. “Una meta futura es llevar los estudios clínicos adonde está el paciente, en vez de que el paciente vaya al estudio clínico” dijo, además de indicar que para esto, la telemedicina tendrá seguramente un papel importante.
La mayoría de los investigadores encuestados señalaron que sus instituciones establecieron normas sobre la pandemia de la COVID-19. En el 75 % de los programas de los encuestados, el personal de investigación trabajó a distancia de forma obligatoria.
En la encuesta se observó que fue común que se retrasaran las actividades de investigación clínica. En la mayoría de los programas de los encuestados, se suspendieron los exámenes de detección del cáncer o la inscripción para algunos estudios clínicos, como los que solo se realizaban con fines de investigación.
“Muchos centros oncológicos dieron prioridad a la inscripción de pacientes en los estudios clínicos según la gravedad de la enfermedad, las opciones de tratamiento disponibles en cada caso y el personal con que contaba cada centro”, comentó el doctor Waterhouse.
Estos resultados concuerdan con los resultados de una segunda encuesta a 36 investigadores realizada entre el 23 de marzo y el 3 de abril. La inscripción de pacientes en estudios clínicos activos de cáncer disminuyó durante el período de la encuesta. Pocas instituciones continuaron con la inscripción de pacientes a un ritmo normal: solo 20 % en los Estados Unidos y 14 % en Europa.
Estudios clínicos en la comunidad
En los Estados Unidos, la repercusión de la pandemia en los estudios clínicos de cáncer fue distinta según la forma en que la COVID-19 afectó las zonas de los estudios.
Esto se observó en general en el Programa de Investigación Oncológica Comunitaria del NCI (NCORP), que lleva a cabo estudios clínicos en más de 1000 centros en 43 estados, el Distrito de Columbia, Puerto Rico y Guam. Estos centros están en zonas rurales y urbanas. En el NCORP participan 14 establecimientos designados como centros comunitarios de atención a grupos minoritarios y desatendidos.
Además de incluir estudios clínicos de tratamiento del cáncer, el NCORP comprende estudios clínicos de cáncer sobre prevención, exámenes de detección, tratamiento de los síntomas y prestación de la atención oncológica.
Al comienzo de la pandemia, el NCORP estableció como prioridad brindar atención a los pacientes que recibían tratamiento del cáncer, según la doctora Worta McCaskill-Stevens, jefa del Grupo de Investigación Oncológica y de Estudios Clínicos de Prevención Comunitarios, que incluye al NCORP.
El NCORP recomendó pautas para modificar los estudios clínicos durante la pandemia, como permitir que los pacientes firmaran a distancia los formularios de consentimiento y que las reuniones de seguimiento con los médicos fueran virtuales. Se autorizó que los pacientes que no podían viajar al centro principal de estudios clínicos fueran a otro centro o a un consultorio médico local.
“Los centros que participan en el NCORP son diversos e incluyen ciudades y zonas rurales. De esta forma, el NCI registra información valiosa sobre la capacidad de superación de la comunidad de los investigadores durante las crisis y el compromiso que tienen con la atención y la investigación del cáncer”, explicó la doctora McCaskill-Stevens.
Algunos consultorios oncológicos rurales ya usaban telemedicina y dependieron de este sistema durante la pandemia para seguir ofreciendo la mayor cantidad de consultas clínicas posibles. Para los centros comunitarios de atención a grupos minoritarios y desatendidos ubicados en las ciudades, la situación por la pandemia fue más difícil.
“Dos de los hospitales del NCORP en la ciudad de Nueva York, Columbia y Montefiore, dedicaron los recursos al cuidado de las personas con COVID-19”, indicó la doctora McCaskill-Stevens. “Los medios de comunicación cubrieron la noticia sobre los esfuerzos heroicos del personal médico en estos hospitales”.
Agregó que, en Chicago, el NCORP del condado de Cook se vio obligado a cerrar por un tiempo la unidad de quimioterapia al enterarse de que los miembros del equipo de tratamiento oncológico se podrían haber expuesto al coronavirus.
“La pandemia presenta desafíos a la práctica oncológica establecida”, dijo la doctora McCaskill-Stevens.
Estudios clínicos para niños con cáncer
Al igual que el Centro Clínico de los NIH y otros centros de estudios clínicos, el hospital St. Jude continúa con la inscripción de pacientes que tienen pocas opciones de tratamiento, como los niños con tumores cerebrales y otros tipos de cáncer muy malignos, en los estudios clínicos de terapias nuevas.
Sin embargo, por el momento, en el hospital se dejó de inscribir a pacientes nuevos en los estudios clínicos que no evalúan un tratamiento. Esto incluye los estudios sobre la prevención del cáncer y la supervivencia, comenta la doctora Elizabeth Fox, que supervisa los estudios clínicos de investigación en St. Jude.
Otra forma en que St. Jude trató de evitar la propagación de la COVID-19 fue pedir que solo un familiar o tutor acompañara al niño durante las consultas hospitalarias. Fue necesario establecer el requisito de un solo cuidador y reconocemos que se trata de un sacrificio para la familia”, señaló la doctora Fox, que explicó que St. Jude ofrece tratamiento de cáncer a pacientes que provienen de todos los Estados Unidos.
“Para cualquier familia, el diagnóstico de cáncer infantil causa un estrés enorme”, continuó. “La pandemia se suma a la incertidumbre que las familias ya sienten.”
Al contar con menos personal en los hospitales, hubo que retrasar evaluaciones estándar para los niños que participan en estudios clínicos de nuevos tratamientos. “Es comprensible que haya familias que se pregunten si los niños podrán recibir los tratamientos programados a tiempo para saber si estos son eficaces”, dijo la doctora Fox. “Esta es otra fuente de estrés”.
Los investigadores de St. Jude también comenzaron el envío directo de medicamentos orales a las familias de los pacientes que están probando estos medicamentos, lo cual les ahorra un viaje al hospital. “Queremos continuar haciendo esto con las futuras pruebas de medicamentos orales”, mencionó la doctora Fox.
Supervisión de los estudios clínicos
Los estudios clínicos se controlan para asegurar la calidad de los datos recopilados por los investigadores y el cumplimiento de las reglamentaciones sobre la investigación clínica. Antes de la pandemia, los supervisores o monitores de estudios clínicos solían viajar hasta los centros de estudios clínicos para ingresar a las computadoras y revisar los datos de los estudios, como las historias clínicas electrónicas de los pacientes.
Sin embargo, en respuesta a la pandemia, el Programa de Evaluación de Tratamientos del Cáncer (CTEP) del NCI incorporó métodos para la supervisión de los estudios a distancia.
“Antes de la COVID-19, muy pocas instituciones que administraban los estudios patrocinados por el NCI permitían que los auditores accedieran a distancia a las historias clínicas electrónicas”, comentó Gary L. Smith, a cargo de la División de Supervisión de Estudios Clínicos (CTMB) del NCI, que establece pautas y normas sobre el funcionamiento de los estudios clínicos que patrocina el NCI. “En definitiva, estamos observando que cada vez hay más auditorias a distancia”.
Ahora que la mayoría de las historias clínicas están disponibles en formato electrónico y es posible acceder a estas por computadora desde cualquier lugar, “no tiene sentido hacer que los supervisores viajen hasta cada centro”, explicó Smith. “No creo que podamos sustituir por completo las auditorías en los centros, pero podemos aumentar la cantidad de este tipo de auditorías para supervisar a distancia”.
Hace poco, algunos centros comenzaron a permitir las auditorías en persona, añadió. Pero los centros tienen un espacio separado del lugar donde están los pacientes para disminuir la posibilidad de transmisión de la COVID-19.
“Nuestra preocupación principal”, dijo Smith, “siempre fue la seguridad de los supervisores que viajan a los centros y la seguridad de los pacientes en los estudios clínicos que se podrían exponer al coronavirus por un supervisor que tiene la infección pero es asintomático”.
“Nuestra preocupación principal”, dijo Smith, “siempre fue la seguridad de los supervisores que viajan a los centros y la seguridad de los pacientes en los estudios clínicos que se podrían exponer al coronavirus por un supervisor que tiene la infección pero es asintomático”.
Ampliación del alcance de los estudios clínicos
Viajar a los centros de los estudios clínicos siempre ha sido una carga para los pacientes que participan en los estudios y esto contribuye a crear desigualdades entre las personas que reciben servicios de los estudios, destacó el doctor Eric J. Small, que estudia y trata a pacientes de cáncer de próstata en la Universidad de California en San Francisco (UCSF).
Pero la pandemia creó una oportunidad para examinar las prácticas que se usan en la actualidad en los estudios clínicos, que incluyen la frecuencia con que los pacientes necesitan una evaluación en persona, según escribió el doctor Small en un comentario sobre la necesidad urgente de transformar los estudios clínicos del cáncer.
“Aprendimos que podemos hacer mucho más de lo que pensábamos a distancia”, comentó el doctor Small. “Es obvio que hay situaciones en las que tenemos que ver al paciente, pero pienso que aprendimos que contar con la flexibilidad de usar telemedicina es importante”.
Añadió que, “Además, aprendimos que evaluar la respuesta del paciente a los tratamientos cada 6 semanas tal vez es demasiado seguido y que no se pierde nada si lo hacemos cada 3 meses”.
Durante la pandemia, el doctor Small y sus colegas en la UCSF cambiaron de forma muy notable la estrategia de tratamiento de los pacientes de cáncer, incluso de los que participaban en estudios clínicos. Las decisiones sobre la atención dependían, explicó, de que el profesional de la salud considerara que el tratamiento del paciente fuese esencial. Estos pacientes continuaron las consultas en el hospital y se inscribieron en estudios clínicos.
Durante la pandemia, el doctor Small y sus colegas en la UCSF cambiaron de forma muy notable la estrategia de tratamiento de los pacientes de cáncer, incluso de los que participaban en estudios clínicos. Las decisiones sobre la atención dependían, explicó, de que el profesional de la salud considerara que el tratamiento del paciente fuese esencial. Estos pacientes continuaron las consultas en el hospital y se inscribieron en estudios clínicos.
La pandemia no tuvo un efecto tan fuerte en San Francisco en comparación con otras ciudades de la costa este del país, y el Centro Oncológico Integral Familiar Helen Diller de UCSF se encuentra en “modo de recuperación”, explicó el doctor Small. “La mayoría de nuestros estudios clínicos que se habían suspendido, incluso los de pacientes hospitalizados de riesgo alto, se volvieron a abrir y aceptan inscripciones de participantes”.
El doctor Small tiene la esperanza de que en los próximos meses y años las lecciones aprendidas durante la pandemia produzcan cambios, como el uso amplio de la telemedicina. Esto daría mayor acceso a los estudios clínicos a las personas “que no tienen los medios para subir a un automóvil y pasar todo el día conduciendo a una consulta médica”.
Agregó, “Mi esperanza es que incluyamos a más grupos desatendidos, en especial, los que están en zonas rurales”.






















.png)










No hay comentarios:
Publicar un comentario